
【题目】在2KMnO4+16HCl=2KCl+2MnCl2+5Cl2↑+8H2O反应中
(1)该反应的氧化剂是 , 氧化产物是
(2)该反应的离子方程式为
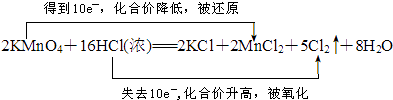
(3)请用“双线桥法”标出该反应电子转移的方向和数目.
(4)该反应氧化剂与还原剂的物质的量之比为 .
【答案】
(1)KMnO4,Cl2
(2)2MnO4﹣+16H+=2Mn2++5Cl2↑+8H2O
(3)
(4)1:5
【解析】解:(1)2KMnO4+16HCl═2MnCl2+5Cl2↑+8H2O+2KCl中,Mn元素的化合价降低,KMnO4为氧化剂,Cl元素的化合价升高,被氧化,则氧化产物为Cl2,
所以答案是:KMnO4;Cl2;
(2)2KMnO4+16HCl(浓)═2KCl+2MnCl2+5Cl2↑+8H2O,离子方程式为:2MnO4﹣+16H+=2Mn2++5Cl2↑+8H2O,
所以答案是:2MnO4﹣+16H+=2Mn2++5Cl2↑+8H2O;
(3)2KMnO4+16HCl(浓)═2KCl+2MnCl2+5Cl2↑+8H2O中Mn元素化合价降低,被还原,KMnO4为氧化剂,Cl元素化合价升高,被氧化,HCl为还原剂,反应中Mn得到2×5e﹣,Cl失去10e﹣,电子转移数目和方向可表示  ,
,
所以答案是:  ;
;
(4)反应中,化合价升高是元素是盐酸中的氯元素,所以盐酸是还原剂,16mol的盐酸中只有10mol做还原剂,化合价降低的元素是锰元素,所以高锰酸钾是氧化剂,氧化剂与还原剂的物质的量比为1:5,
所以答案是:1:5.


 课堂全解字词句段篇章系列答案
课堂全解字词句段篇章系列答案 步步高口算题卡系列答案
步步高口算题卡系列答案科目:高中化学 来源: 题型:
【题目】在电解质溶液的导电性装置(如图所示)中,若向某一电解质溶液中逐滴加入另一溶液时,则灯泡由亮变暗,至熄灭后又逐渐变亮的是( )
A.盐酸中逐滴加入食盐溶液
B.硫酸中逐滴加入氢氧化钠溶液
C.石灰乳中逐滴加入稀盐酸
D.硫酸中逐滴加入氢氧化钡溶液
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】氧化还原反应与四种基本类型反应的关系如图所示,则下列化学反应属于阴影部分的是( )
A.Cl2+2KBr═Br2+2KCl
B.2NaHCO3 ![]() Na2CO3+H2O+CO2↑
Na2CO3+H2O+CO2↑
C.4Fe(OH)2+O2+2H2O═4Fe(OH)3
D.2Na2O2+2CO2═2Na2CO3+O2↑
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列离子方程式正确的是( )
A.氧化镁与稀盐酸混合:O2﹣+2 H+═H2O
B.碳酸钠溶液和石灰乳反应:CO32﹣+Ca2+═CaCO3↓
C.稀硫酸与锌反应:2 H++Zn═Zn2++H2↑
D.向沸水中滴加FeCl3溶液制备Fe(OH)3胶体:Fe3++3H2O ![]() Fe(OH)3↓+3H+
Fe(OH)3↓+3H+
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】苯是一种重要的有机化工原料,广泛用于合成橡胶、塑料和医药等方面。下列关于苯的叙述不正确的是 ( )
A. 分子式为C6H6 B. 属于不饱和烃
C. 能在空气中燃烧 D. 无色无毒的液体
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】铝自然形成的氧化膜易脱落.以硫酸为电解液,分别以石墨和铝材做阴、阳极材料,经过电解处理形成的氧化铝膜,抗蚀能力强.其制备的简要流程如图.下列用来解释流程中反应的方程式不正确的是( ) 
A.碱洗目的是除去铝材表面的自然氧化膜:2OH﹣+Al2O3═2AlO2﹣+H2O
B.碱洗时铝材表面会出现气泡:2Al+2OH﹣+2H2O═2AlO2﹣+3H2↑
C.获得耐蚀铝材的电极反应为:4Al﹣12e﹣+3O2═2Al2O3
D.用稀氨水洗去耐蚀铝材表面的酸:NH3H2O+H+═NH4++H2O
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】将标准状况下22.4L的HCl溶于水配成200mL的溶液,所得溶液的物质的量浓度为;同温、同压下等质量的NO2和NO气体,它们所占的体积比为 , 所含氧元素的物质的量之比为 .
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】25℃,101kPa时,强酸与强碱的稀溶液发生中和反应的中和热为57.3kJmol﹣1 , 辛烷的燃烧热为5518kJmol﹣1 . 下列热化学方程式书写正确的是( )
A.2H+(aq)+SO42﹣(aq)+Ba2+(aq)+20H﹣(aq)=BaSO4(s)+2H20(l);△H=﹣114.6 kJ?mol﹣1
B.KOH(aq)+ ![]() H2SO4(aq)=
H2SO4(aq)= ![]() K2SO4(aq)+H2O(1);△H=﹣57.3kJ?mol﹣1
K2SO4(aq)+H2O(1);△H=﹣57.3kJ?mol﹣1
C.C8H8(1)+ ![]() O2(g)=8CO2(g)+9H20(g);△H=﹣5518kJ?mol﹣1
O2(g)=8CO2(g)+9H20(g);△H=﹣5518kJ?mol﹣1
D.2C8H18(g)+2502(g)=16C02(g)+18H20(l),△H=﹣5518 kJ?mol﹣1
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com