
在通常条件下,下列各组物质的性质排列不正确的是()
A. 沸点:乙烷>戊烷>2﹣甲基丁烷
B. 熔点:Al>Na>Na和K的合金
C. 密度:苯<水<1,1,2,2﹣四溴乙烷
D. 热稳定性:HF>HCl>H2S
考点: 晶体的类型与物质熔点、硬度、导电性等的关系;同一周期内元素性质的递变规律与原子结构的关系;同一主族内元素性质递变规律与原子结构的关系.
分析: A.烷烃中碳原子个数越多其熔沸点越高,同分异构体中支链越多其熔沸点越低;
B.金属的金属键越强,其熔点越高,金属键与离子半径成反比,合金熔点高于其任一成分熔点;
C.苯的密度小于1g/mL、水的密度是1g/mL、1,1,2,2﹣四溴乙烷的密度大于1g/mL;
D.元素的非金属性越强,其氢化物的稳定性越强.
解答: 解:A.烷烃中碳原子个数越多其熔沸点越高,同分异构体中支链越多其熔沸点越低,所以这几种烷烃的熔沸点戊烷>2﹣甲基丁烷>乙烷,故A错误;
B.金属的金属键越强,其熔点越高,金属键与离子半径成反比,所以金属键Na<Al,合金熔点高于其任一成分熔点,Na、K合金熔点低于Na,所以熔点Al>Na>Na和K的合金,故B正确;
C.苯的密度小于1g/mL、水的密度是1g/mL、1,1,2,2﹣四溴乙烷的密度大于1g/mL,所以密度苯<水<1,1,2,2﹣四溴乙烷,故C正确;
D.元素的非金属性越强,其氢化物的稳定性越强,非金属性F>Cl>S,则氢化物的稳定性HF>HCl>H2S,故D正确.
故选A.
点评: 本题考查较综合,涉及烷烃物理性质、金属键、密度大小比较、元素周期律等知识点,侧重考查分析判断能力,知道金属键的影响因素、非金属性强弱与氢化物稳定性及其最高价氧化物的水化物酸性关系,题目难度不大.


 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案科目:高中化学 来源: 题型:
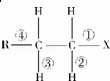
在卤代烃R﹣CH2﹣CH2﹣X中化学键如图所示,则下列说法正确的是( )
|
| A. | 发生水解反应时,被破坏的键是①和③ |
|
| B. | 发生消去反应时,被破坏的键是②和③ |
|
| C. | 发生水解反应时,被破坏的键是① |
|
| D. | 发生消去反应时,被破坏的键是①和② |
查看答案和解析>>
科目:高中化学 来源: 题型:
我国化学家侯德榜根据NaHCO3溶解度比NaCl、Na2CO3、NH4HCO3、NH4Cl都小的性质,运用CO2+NH3+H2O+NaCl=NaHCO3↓+NH4Cl的反应原理制备纯碱.下面是在实验室进行模拟实验的生产流程示意图:
气体A的饱和溶液 A和食盐的饱和溶液
A和食盐的饱和溶液 悬浊液
悬浊液 晶体
晶体 纯碱
纯碱
则下列叙述错误的是()
A. A气体是CO2,B气体是NH3
B. 第Ⅲ步得到的晶体是发酵粉的主要成分
C. 第Ⅲ步操作用到的主要玻璃仪器是烧杯、漏斗、玻璃棒
D. 第Ⅳ步操作的主要过程有溶解、蒸发、结晶
查看答案和解析>>
科目:高中化学 来源: 题型:
A、B、C、D都是中学化学中常见物质,其中A、B、C均含有同一种元素,在一定条件下相互转化关系如图(部分反应中的水已略去).
(1)若A为氯碱工业的产品,C为厨房中的用品.
①反应Ⅲ的离子方程式是 .
②C浓度为0.1mol/L时,pH最接近 .
A.5.6 B.7.0 C.8.4 D.13.0
③B溶液中各离子浓度由大到小顺序是 ,氯碱工业中两种产物可与KI溶液反应制得一种化工原料,若消耗0.1mol KI转移电子0.6mol,则三种物质间反应的离子方程式是 .
(2)若A、D均为单质,且A为气体,D元素的一种红棕色氧化物常用作颜料.
①检验某溶液中含有B的阳离子的方法是 .
②B可作净水剂,其原理是 (用方程式表示).在使用时发现B不能使酸性废水中的悬浮物沉降除去,其原因是 .

查看答案和解析>>
科目:高中化学 来源: 题型:
实验室用溴和苯在FeBr3催化下制取溴苯,得到粗溴苯后,要用如下操作提纯:(1)蒸馏;(2)水洗;(3)用干燥剂干燥;(4)用10%的NaOH溶液洗涤.正确的操作顺序是()
A. (1)(2)(3)(4) B. (4)(2)(3)(1) C. (4)(1)(2)(3) D. (2)(4)(2)(3)(1)
查看答案和解析>>
科目:高中化学 来源: 题型:
为了检验某溴代烃中的溴元素,现进行如下操作,其中合理的是()
A. 取溴代烃少许,加入AgNO3溶液
B. 取溴代烃少许与NaOH水溶液共热,然后加入AgNO3溶液
C. 取溴代烃少许与NaOH乙醇溶液共热后,加入稀硝酸酸化后,再加入AgNO3溶液
D. 取溴代烃少许与NaOH水溶液共热后,加入稀硝酸酸化后,再加入AgNO3溶液
查看答案和解析>>
科目:高中化学 来源: 题型:
下表中评价不合理的是 ( )。
| 选项 | 化学反应及其离子方程式 | 评价 |
| A | 向碳酸镁中加入稀盐酸:CO | 错误,碳酸镁不应写成离子形式 |
| B | 向硫酸铜溶液中加入氢氧化钡溶液:Ba2++SO | 正确 |
| C | 向FeCl3溶液中加入Fe粉:Fe3++Fe===2Fe2+ | 错误,离子所带电荷不守恒且电子得失不相等 |
| D | 以石墨作电极电解氯化钠溶液:2Cl-+2H2O | 正确 |
查看答案和解析>>
科目:高中化学 来源: 题型:
天然维生素P(结构简式如图)存在于槐树花蕾中,它是一种营养增补剂。关于维生素P的叙述错误的是 ( )。
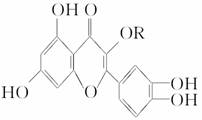
A.可以和溴水反应
B.可用有机溶剂萃取
C.分子中有三个苯环
D.1 mol维生素P可以和4 mol NaOH反应
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com