
| 实验操作 | 预期现象和结论 |
| | |
| | |
| 实验操作 | 预期现象和结论 |
| 向溶液B中滴加少量Ba(NO3)2溶液。(1分) | 如果产生白色沉淀,说明原固体混合物中含有K2SO4;(1分) 如果没有白色沉淀产生,说明原固体混合物中不含K2SO4,(含有NaCl或NH4Cl。) (1分) |
| 取少量原固体混合物于试管底部,(1分) 将试管套入试管夹,用火柴点燃酒精灯,充分加热试管。(1分) | 如果试管底部有固体残留,说明混合物中含有NaCl;(1分) 如果试管底部无固体残留,说明混合物中含有NH4Cl;(1分) |
| 实验操作 | 预期现象和结论 |
| 向溶液B中滴加少量Ba(NO3)2溶液。 | 如果产生白色沉淀,说明原固体混合物中含有K2SO4; 如果没有白色沉淀产生,说明原固体混合物中不含K2SO4,(含有NaCl或NH4Cl。) |
| 取少量原固体混合物于试管底部,(1分) 将试管套入试管夹,用火柴点燃酒精灯,充分加热试管。 | 如果试管底部有固体残留,说明混合物中含有NaCl; 如果试管底部无固体残留,说明混合物中含有NH4Cl; |


 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案科目:高中化学 来源:不详 题型:实验题
查看答案和解析>>
科目:高中化学 来源:不详 题型:填空题
查看答案和解析>>
科目:高中化学 来源:不详 题型:实验题
 如下的问题,探究。请你协助该小组的同学完成下列研究。
如下的问题,探究。请你协助该小组的同学完成下列研究。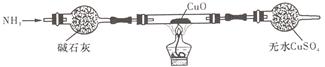
 能被NH3还原吗?
能被NH3还原吗? 红色物质是Cu,也有同学认为NH3与CuO反应生成的红色物质
红色物质是Cu,也有同学认为NH3与CuO反应生成的红色物质 是Cu和A的混合物。请你设计一个简单的实验检验NH3与CuO反应中生成的红色物质中是否含有A______________________________________________________。
是Cu和A的混合物。请你设计一个简单的实验检验NH3与CuO反应中生成的红色物质中是否含有A______________________________________________________。查看答案和解析>>
科目:高中化学 来源:不详 题型:实验题
查看答案和解析>>
科目:高中化学 来源:不详 题型:实验题
| 编号 | 操作方法 | 实验目的 |
| A | | 探究铁在干燥空气中的生锈情况 |
| B | 放入铁钉,注入蒸馏水浸没铁钉,并用植物油液封 | |
| C | | 探究铁在有空气和水封时的生锈情况 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| A.在标准状况下,1 mol任何物质的体积为22.4 L |
| B.等物质的量浓度的盐酸和硫酸中,H+的物质的量浓度也相等 |
| C.1 mol H2和1 mol He中,所含的分子数相同、原子数相同,质量也相同 |
| D.体积为6 L的O2,其质量可能为8 g |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| A.乙酸具有挥发性 |
| B.乙酸有刺激性气味 |
| C.乙酸是有机酸而碳酸是无机酸 |
| D.乙酸能与碳酸氢钠反应放出CO2 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:计算题

查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com