
下列有关化学实验操作及安全的说法正确的是
A.用酒精灯给锥形瓶加热来浓缩溶液
B.实验室不能采用向下排空气法收集CO
C.实验室用碳酸钙和稀盐酸反应,气体产物经碱石灰干燥后可得纯净干燥的CO2
D.氢氧化钙溶液存放在配有磨口塞的玻璃瓶中
 期末集结号系列答案
期末集结号系列答案科目:高中化学 来源:2015-2016学年山西省高一上第一次月考化学试卷(解析版) 题型:选择题
以下转化不能通过一步反应实现的是
A.CuO→Cu(OH)2 B.CO2→Na2CO3
C.Fe→FeCl2 D.CaCO3→Ca(NO3)2
查看答案和解析>>
科目:高中化学 来源:2015-2016学年内蒙古奋斗中学高二上9月质检化学试卷(解析版) 题型:选择题
已知反应:①2C(s)+O2(g)=2CO(g) ΔH=-221 kJ/mol;②稀溶液中,H+(aq)+OH-(aq)=H2O(l) ΔH=-57.3 kJ/mol。下列结论正确的是
A.碳的燃烧热110.5 kJ/mol
B.①的反应热为221 kJ/mol
C.稀醋酸与稀NaOH溶液反应的中和热为57.3 kJ/mol
D.稀盐酸与稀NaOH溶液反应的中和热为57.3 kJ/mol
查看答案和解析>>
科目:高中化学 来源:2016届江西省高三上学期第三次月考化学试卷(解析版) 题型:选择题
有一粗硅,含杂质铁,取等质量的样品分别投入足量的稀盐酸和足量的稀氢氧化钠溶液中,放出等量的H2,则该粗硅中铁和硅的关系正确的是(提示:Si+2NaOH+H2O===Na2SiO3+2H2↑)
A.物质的量之比为:1∶1 B.质量之比为4∶1
C.物质的量之比为1∶2 D.质量之比为2∶1
查看答案和解析>>
科目:高中化学 来源:2015-2016学年重庆一中高一上学期10月月考化学试卷(解析版) 题型:实验题
(原创)(20分)重庆一中某化学兴趣小组,欲在常温常压下,用一定质量的铜镁合金与足量稀盐酸反应,利用下图装置,测定样品中铜的质量分数。
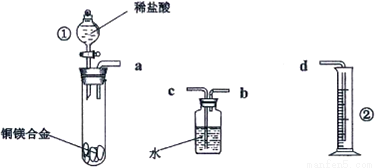
A B C
(1)实验反应原理:写出镁与稀盐酸发生反应的化学方程式________________
(2)仪器识别:写出上图中仪器①、②的名称:①_________②__________
(3)装置连接:a→___________→___________→d
(4)A中反应已经进行完毕的现象为__________________________
(5)实验中,该兴趣小组同学测得以下数据
a.反应前样品铜镁合金的质量,记为m1 g
b.反应结束后,经过处理后的残余固体的质量,记为m2 g
c.经过一系列正确的操作后,读取量筒中的水的体积,记为V mL
d.查阅资料,常温常压下,H2的密度为ρ g/L
四位同学分成甲、乙两个小组,甲组同学利用重量法为思路,请合理选择以上数据,列式求铜的质量分数:________×100%;乙组同学利用排水法测量气体体积为思路,请合理选择以上数据,列式求铜的质量分数:________×100%
(6)误差分析环节中指导教师提出,甲、乙两组同学的思路中,会有很多因素导致测得的铜的质量分数出现误差,现将可能导致误差的因素罗列如下,并回答相关问题
a.读取量筒中水的体积时,未等装置中气体恢复至室温
b.读取量筒中水的体积时,俯视量筒
c.实验开始前,没有检查装置气密性,然而装置实际是漏气的
d.B瓶中残留的空气的干扰
e.未除去样品铜镁合金表面的氧化膜便进行称量
f.未对反应中挥发出的HCl气体进行除杂处理
g.未对反应后剩余的残余物进行洗涤
h.未考虑B、C装置间连接导管中残留的水
导致铜的质量分数大于理论值的原因可能是___________________(填符号a~h)
导致铜的质量分数小于理论值的原因可能是___________________(填符号a~h)
查看答案和解析>>
科目:高中化学 来源:2016届黑龙江省高三上学期期中测试化学试卷(解析版) 题型:选择题
下列关于离子的检验方法一定正确的是
A.向某溶液中滴加BaCl2溶液,有白色沉淀生成,再滴加足量稀HNO3,沉淀不溶解, 说明原溶液中一定含有Ag+
B.向某溶液中滴加浓NaOH溶液,加热,产生的气体使湿润的红色石蕊试纸变蓝色,说明原溶液中含NH4+
C.向某溶液中滴加足量稀盐酸,产生使澄清石灰水变浑浊的气体,说明原溶液中一定含CO32-
D.用铂丝蘸取某溶液在无色火焰上灼烧,直接观察火焰颜色未见紫色,说明原溶液中不含K+
查看答案和解析>>
科目:高中化学 来源:2016届湖北省、宜昌一中高三上10月联考化学试卷(解析版) 题型:选择题
短周期元素X、Y、Z、W的原子序数依次增大,X和Z同主族,Y和W同主族,原子半径X小于Y,四种元素原子最外层电子数之和为14。下列叙述正确的是
A.同周期元素中W的最高价氧化物对应水化物的酸性最强
B.氢化物的热稳定性:HnY>HnW
C.Y和X、Z和X组成的常见化合物中化学键的类型相同
D.原子半径的大小顺序: rW>rZ>rY>rX
查看答案和解析>>
科目:高中化学 来源:2016届重庆市高三上学期9月月考化学试卷(解析版) 题型:选择题
右图表示在某溶液中滴加Ba(OH)2溶液时,生成的沉淀的物质的量随Ba(OH)2溶液的体积变化关系。该溶液的成分可能是

A.NH4Al(SO4)2
B.KAl(SO4)2
C.Al2(SO4)3
D.Na2SO4与NaAlO2组成的混合物
查看答案和解析>>
科目:高中化学 来源:2016届四川省雅安市高三9月月考化学试卷(解析版) 题型:填空题
(本题共14分)常见的五种盐X、Y、Z、M、N,它们的阴离子可能是SO、Cl-、NO、CO,阳离子可能是Ag+、NH、Na+、Al3+、Cu2+、Ba2+、Fe3+,已知:
①M的焰色反应呈黄色。
②五种盐均溶于水,水溶液均为无色。
③X的溶液呈中性,Y、Z、N的溶液呈酸性,M的溶液呈碱性。
④若在这五种盐的溶液中分别加入Ba(NO3)2溶液,只有X、Z的溶液不产生沉淀。
⑤若在这五种盐的溶液中,分别加入氨水,N和Z的溶液中生成沉淀,继续加氨水,Z中沉淀消失。
⑥把X的溶液分别加入到Y、Z、N的溶液中,均能生成不溶于稀硝酸的沉淀。
请回答下列问题:
(1)五种盐中,一定不含有的阳离子是_______;所含阴离子相同的两种盐的化学式是__________________。
(2)M的化学式为_________________________,M溶液显碱性的原因是_______________________(用离子方程式表示)。
(3)X和Z的溶液反应的离子方程式是_________________________________;N和氨水反应的离子方程式是____________________________________。
(4)若要检验Y中所含的阳离子,正确的实验方法是______________________。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com