
 xP (g) +2Q (g)��5min��Ӧ�ﵽƽ�⣬��֪M��ת����Ϊ50%��P�ķ�Ӧ����Ϊ0.15mol��L��1��min��1��������˵����ȷ���ǣ���
xP (g) +2Q (g)��5min��Ӧ�ﵽƽ�⣬��֪M��ת����Ϊ50%��P�ķ�Ӧ����Ϊ0.15mol��L��1��min��1��������˵����ȷ���ǣ���| A������ʽ��x=2 |
| B����ƽ���������ѹǿ�Ƿ�Ӧ��ʼʱ��2�� |
| C�����������ٳ���3.0molM��2.5molN������ƽ��ʱQ �����������С |
| D�������ڻ��������ܶȲ��ٱ仯��ƽ����Է����������ٱ仯������Ϊ�ﵽƽ��״̬�ı�־ |
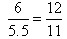 ��B����ȷ�����������ٳ���3.0molM��2.5molN���൱������ѹǿ���ƻ����淴Ӧ�����ƶ�������Q �����������С��C��ȷ���ܶ��ǻ�����������������ݻ��ı�ֵ���ڷ�Ӧ�������������ݻ�ʼ���Dz���ģ�����ѡ��D����ȷ����ѡC��
��B����ȷ�����������ٳ���3.0molM��2.5molN���൱������ѹǿ���ƻ����淴Ӧ�����ƶ�������Q �����������С��C��ȷ���ܶ��ǻ�����������������ݻ��ı�ֵ���ڷ�Ӧ�������������ݻ�ʼ���Dz���ģ�����ѡ��D����ȷ����ѡC��


| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ������ ���ͣ���ѡ��
 2C(g)����H<0������ʼʱ��M��N�ݻ���ͬ������˵����ȷ���ǣ� ��
2C(g)����H<0������ʼʱ��M��N�ݻ���ͬ������˵����ȷ���ǣ� ��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ������ ���ͣ������
 2SO3������д���пհף�
2SO3������д���пհף�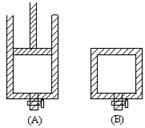
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ������ ���ͣ���ѡ��
 Z(g) �SH��0����60s�ﵽƽ�⣬����0.3mol Z������˵����ȷ����
Z(g) �SH��0����60s�ﵽƽ�⣬����0.3mol Z������˵����ȷ����| A����YŨ�ȱ仯��ʾ�ķ�Ӧ����Ϊ0.0005mol��L-1��s-1 |
| B����XŨ�ȱ仯��ʾ�ķ�Ӧ����Ϊ0.0005mol��L-1��s-1 |
| C������λʱ��������a mol Y��ͬʱ������2a mol X����Ӧ�ﵽƽ��״̬ |
| D���������¶ȣ�����Ӧ���������淴Ӧ���ʼ�С |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ������ ���ͣ������
 H2��g����CO��g����
H2��g����CO��g���� CH3OH��g����һ�������£������Ϊ1 L���ܱ������г���1 mol CO��3 mol H2����Ӧ�ﵽƽ��״̬ʱ��CO��ƽ��ת����Ϊ75%��
CH3OH��g����һ�������£������Ϊ1 L���ܱ������г���1 mol CO��3 mol H2����Ӧ�ﵽƽ��״̬ʱ��CO��ƽ��ת����Ϊ75%���鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ������ ���ͣ���ѡ��
 2C2 (g)+2D(g)��������Ϊ��Ӧ�ﵽƽ��ı�־��(C )
2C2 (g)+2D(g)��������Ϊ��Ӧ�ﵽƽ��ı�־��(C )�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ������ ���ͣ������
 2C(g) ��H��0
2C(g) ��H��0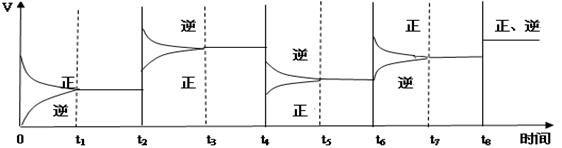
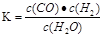
| A�������������ƽ����Է�����������ʱ����仯 |
| B������(H2O)������(H2) |
| C��������������ܶȲ���ʱ����仯 |
| D���������ܵ����ʵ�������ʱ����仯 |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ������ ���ͣ������
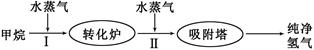
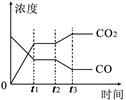
 H2(g)��CO2(g)���÷�Ӧ�Ļ�ѧƽ�ⳣ������ʽΪK= ����Ӧ��ƽ�ⳣ�����¶ȵı仯���±���
H2(g)��CO2(g)���÷�Ӧ�Ļ�ѧƽ�ⳣ������ʽΪK= ����Ӧ��ƽ�ⳣ�����¶ȵı仯���±���| �¶�/�� | 400 | 500 | 830 | 1000 |
| ƽ�ⳣ��K | 10 | 9 | 1 | |
| ʵ���� | n(CO) | n(H2O) | n(H2) | n(CO2) |
| A | 1 | 5 | 2 | 3 |
| B | 2 | 2 | 1 | 1 |
| C | 0.5 | 2 | 1 | 1 |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ������ ���ͣ���ѡ��
| A����Ӧ����һ��ƽ��״̬����ʱ��Ӧ�Ѿ�ֹͣ |
| B���ﵽƽ��״̬ʱ������Ӧ���ʺ��淴Ӧ������� |
| C���ﵽƽ��״̬ʱ����Ӧ���������Ũ�ȶ����ٸı� |
| D�����ٷ�Ӧ�����п����ԣ�ֻ���еij̶�С���еij̶ȴ� |
�鿴�𰸺ͽ���>>
����ѧУ��ѡ - ��ϰ���б� - �����б�
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com