
| A. | Al3+、S2-、Na+、Cl- | B. | K+、Fe3+、S2-、OH- | ||
| C. | Ba2+、HCO3-、Fe3+、H+ | D. | Na+、Al3+、SO42-、NO3- |
分析 离子之间不反应生成气体、沉淀、弱电解质或发生氧化还原反应、双水解反应、络合反应的就能大量共存,据此分析解答.
解答 解:A.Al3+、S2-发生双水解反应生成氢氧化铝沉淀和硫化氢气体,所以不能大量共存,故A错误;
B.Fe3+、S2-发生双水解反应,且Fe3+、OH-生成氢氧化铁沉淀,所以不能大量共存,故B错误;
C.HCO3-、Fe3+发生双水解反应,且HCO3-、H+发生复分解反应,所以不能大量共存,故C错误;
D.这几种离子之间不反应,所以能大量共存,故D正确;
故选D.
点评 本题考查离子共存,为高频考点,侧重考查双水解反应,明确离子性质及离子反应条件是解本题关键,熟练掌握哪些离子之间易发生双水解,题目难度不大.


 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案科目:高中化学 来源: 题型:填空题
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | FeO不稳定,在空气中加热迅速被氧化成Fe2O3 | |
| B. | 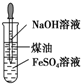 由图示操作可制取Fe(OH)2 | |
| C. | Fe3O4、Fe(OH)3都可以由化合反应制得 | |
| D. | Fe(OH)3胶体呈红褐色、透明,能发生丁达尔现象 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 3mol/L | B. | 2mol/L | C. | 4mol/L | D. | 5mol/L |
查看答案和解析>>
科目:高中化学 来源: 题型:多选题
| A. | 用铂作催化剂 | B. | 降低温度 | ||
| C. | 缩小体积增大压强 | D. | 增大接触面积 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
| 氟 | 氯 | 溴 | 碘 | |
| 第一电离能(kJ/mol) | 1681 | 1251 | 1140 | 1008 |
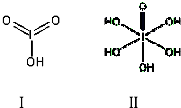
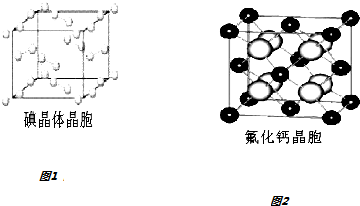
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 1:1 | B. | 1:5 | C. | 1:9 | D. | 2:3 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com