
分析 (1)①高温条件下,CO和氧化铁发生氧化还原反应生成Fe和二氧化碳;
②铁粉遇到高温水蒸气发生反应生成四氧化三铁和氢气;
(2)铝单质与氢氧化钠溶液反应生成四羟基合铝酸钠和氢气.
解答 解:(1)①高温条件下,CO和氧化铁发生氧化还原反应生成Fe和二氧化碳,化学反应方程式为Fe2O3+3CO$\frac{\underline{\;高温\;}}{\;}$2Fe+3CO2,
故答案为:Fe2O3+3CO$\frac{\underline{\;高温\;}}{\;}$2Fe+3CO2;
铁粉遇到高温水蒸气发生反应生成四氧化三铁和氢气,反应为3Fe+4H2O(g)$\frac{\underline{\;高温\;}}{\;}$Fe3O4+4H2↑;
故答案为:3Fe+4H2O(g)$\frac{\underline{\;高温\;}}{\;}$Fe3O4+4H2↑;
(2)铝单质与氢氧化钠溶液反应生成四羟基合铝酸钠和氢气,反应的离子方程式为2Al+2OH-+6H2O=[Al(OH)4]-+3H2↑;AlCl3与氨水反应的离子方程式为:Al3++3NH3.H2O=Al(OH)3+3NH+,
故答案为:2Al+2OH-+6H2O=[Al(OH)4]-+3H2↑.
点评 本题考查离子方程式、化学方程式的书写,明确物质性质是解本题关键,注意:有些化学反应与反应物的量、反应物浓度、反应条件有关,题目难度不大.


科目:高中化学 来源: 题型:选择题
| A. | ①②⑦ | B. | ①②③⑥ | C. | ①②⑥⑦ | D. | ①②④⑤ |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
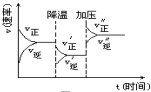 如图是可逆反应A+2B?2C+3D的化学反应速率与化学平衡随外界条件改变(先降温后加压)而变化的情况,由此可推断( )
如图是可逆反应A+2B?2C+3D的化学反应速率与化学平衡随外界条件改变(先降温后加压)而变化的情况,由此可推断( )| A. | 逆反应是放热反应 | B. | 正反应是放热反应 | ||
| C. | 若A、B是气体,则D一定是气体 | D. | A、B、C、D均为气体 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | SiO2(CuO):HCl | B. | MgO(Al2O3):NaOH溶液 | ||
| C. | Na2SiO3溶液(Na2CO3):过量的CO2 | D. | CO2(HCl):饱和NaHCO3溶液 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 使pH试纸呈红色的溶液:I-、NO3-、SO42-、Na+ | |
| B. | 常温下,在c(H+)/c(OH-)=1×1012的溶液:NH4+、Mg2+、C1-、K+ | |
| C. | 加入铝粉放出氢气的溶液:Na+、Cl-、NH4+、NO3- | |
| D. | 使无色酚酞试液显红色的溶液:S2-、K+、HCO3-、Al3+ |
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
查看答案和解析>>
科目:高中化学 来源: 题型:实验题
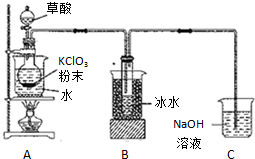 二氧化氯(ClO2)是一种高效消毒剂,沸点为11℃.用KClO3粉末与草酸(H2C2O4)在60℃时反应可生成ClO2等物质,实验装置如图所示:
二氧化氯(ClO2)是一种高效消毒剂,沸点为11℃.用KClO3粉末与草酸(H2C2O4)在60℃时反应可生成ClO2等物质,实验装置如图所示:查看答案和解析>>
科目:高中化学 来源: 题型:解答题
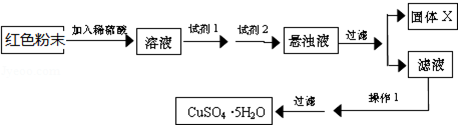
| 物质 | Cu(OH)2 | Fe(OH)2 | Fe(OH)3 |
| 开始沉淀pH | 6.0 | 7.5 | 1.4 |
| 沉淀完全pH | 13 | 14 | 3.7 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com