
| ������� | ��ʼʱ���������ʵ���/mol | ��ƽ�������ϵ �����ı仯 | |||
| CO | H2O | CO2 | H2 | ||
| �� | 1 | 4 | �ų�������32.8 kJ | ||
| �� | 1 | 4 | �����仯��Q | ||
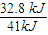 ×1mol=0.8mol��CO��ת����Ϊ
×1mol=0.8mol��CO��ת����Ϊ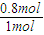 ×100%=80%����A��ȷ��
×100%=80%����A��ȷ��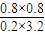 =1��
=1��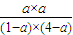 �����a=0.8
�����a=0.8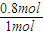 ×100%=80%����B��ȷ��
×100%=80%����B��ȷ��

 ��ĩ���100�ִ��½����ȫ�Ծ�ϵ�д�
��ĩ���100�ִ��½����ȫ�Ծ�ϵ�д�
| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
| 1 |
| 3 |
| 1 |
| 3 |
| 1 |
| 3 |
| 1 |
| 3 |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
 ��2010?������ģ�⣩����̼����ȼ�ϵ���������ڵ�̼����Ϊ����ʵ�ȼ�ϵ�أ��乤��ԭ����ͼ��ʾ��
��2010?������ģ�⣩����̼����ȼ�ϵ���������ڵ�̼����Ϊ����ʵ�ȼ�ϵ�أ��乤��ԭ����ͼ��ʾ��| 1 |
| 2 |
| 1 |
| 2 |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
| A���÷�Ӧ�ġ�S��0 | B���÷�Ӧ���κ��¶��¾����Է����� | C���������г�������He��ƽ��������Ӧ�����ƶ� | D�������¶�ƽ��������Ӧ�����ƶ� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
| 1 |
| 2 |
| 1 |
| 2 |
| A��+41.2 kJ?mol-1 |
| B��-41.2 kJ?mol-1 |
| C��+82.4kJ?mol-1 |
| D��-524.8 kJ?mol-1 |
�鿴�𰸺ͽ���>>
����ѧУ��ѡ - ��ϰ���б� - �����б�
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com