
| A. | 同温、同压下,相同质量的气体都占有相同的体积 | |
| B. | 同温、同压下,相同体积的气体都含有相同数目的分子 | |
| C. | 1molO2中含有1.204×1024个氧原子,在标准状况下占有体积22.4L | |
| D. | 由0.2g H2和8.8g CO2、5.6g CO组成混合气体,其密度是相同状况下O2密度的0.913倍 |
分析 A、根据公式m=nM=$\frac{V}{Vm}$M来判断;
B、根据阿伏伽德罗定律的内容:同温、同压下,相同体积的气体都含有相同数目的分子来回答;
C、根据公式N=nNA结合分子的原子构成情况来回答;
D、根据n=$\frac{m}{M}$计算各气体的物质的量,再根据M=$\frac{m}{n}$计算平均摩尔质量,相同条件下气体密度之比等于其摩尔质量之比,据此计算解答.
解答 解:A、根据公式m=nM=$\frac{V}{Vm}$M,同温、同压下,气体的Vm是相等的,相同质量的气体的物质的量不一定相等,所以占有的体积不一定相等,故A错误;
B、阿伏伽德罗定律:同温、同压下,相同体积的气体都含有相同数目的分子,故B正确;
C、1molO2中含有2mol级1.204×1024个氧原子,在标准状况下占有体积V=nVm=22.4L,故C正确;
D、0.2g H2的物质的量为0.1mol,8.8g CO2的物质的量为0.2mol,5.6gCO的物质的量为0.2mol,故混合气体的平均摩尔质量为$\frac{0.2+8.8+5.6}{0.1+0.2+0.2}$g/mol=29.2g/mol,
混合气体密度是相同条件下O2的密度的$\frac{29.2}{32}$=0.913倍,故D正确.
故选A.
点评 本题考查学生物质的量以及阿伏伽德罗定律的应用知识,注意知识的归纳和梳理是关键,难度中等.


 阅读快车系列答案
阅读快车系列答案科目:高中化学 来源: 题型:选择题
| 选项 | X溶液 | 固体Y | Z溶液 | 现象 |  |
| A | 稀硫酸 | 亚硫酸氢钠 | 品红试剂 | 品红褪色 | |
| B | 浓氨水 | CaO | 紫色石蕊试液 | 溶液变红 | |
| C | 盐酸 | 石灰石 | 硅酸钠溶液 | 出现白色沉淀 | |
| D | 双氧水 | MnO2 | 氢硫酸溶液 | 产生浑浊 |
| A. | A | B. | B | C. | C | D. | D |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
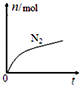
| A. | 该反应的还原剂是Cl- | |
| B. | 消耗1 mol还原剂,转移6 mol电子 | |
| C. | 氧化剂与还原剂的物质的量之比为2:3 | |
| D. | 反应后溶液的酸性明显增强 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
 苯甲酸苯酯是重要的有机合成中间体,工业上用二苯甲酮制备苯甲酸苯酯.
苯甲酸苯酯是重要的有机合成中间体,工业上用二苯甲酮制备苯甲酸苯酯.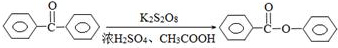
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
| t/℃ | 0 | 10 | 20 | 25 | 40 | 50 | 100 |
| KW/10-14 | 0.114 | 0.292 | 0.681 | 1.01 | 2.92 | 5.47 | 55.0 |
| 化学式 | 电离平衡常数(25℃) |
| HCN | K=5.0×10-10 |
| CH3COOH | K=1.8×10-5 |
| H2CO3 | K1=4.4×10-7,K2=4.7×10-11 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
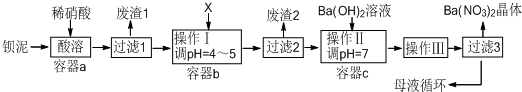
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 1780 | B. | 1220 | C. | -1220 | D. | -1780 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com