
| A. | 加入适量的6mol/L的盐酸 | B. | 加入数滴氯化铜溶液 | ||
| C. | 加入适量蒸馏水 | D. | 加入适量的氯化钠溶液 |
分析 过量的锌片,盐酸完全反应,则加快反应速率又不影响生成氢气的总量,可增大氢离子浓度或增大金属的接触面积、构成原电池等,不改变其氢离子物质的量即可,以此来解答.
解答 解:A.加入适量的6 mol•L-1的盐酸,反应速率加快,生成氢气增多,故A不选;
B.加入数滴氯化铜溶液,锌将铜置换出来形成原电池,反应速率加快,没有改变氢气的总量,故B选;
C.加入适量蒸馏水,浓度变小,反应速率减慢,故C不选;
D.加入适量的氯化钠溶液,反应速率减慢,故D不选;
故选:B.
点评 本题考查影响化学反应速率的因素,注意把握浓度、接触面积对反应速率的影响即可解答,注重基础知识的考查,注意Zn过量盐酸完全反应,题目难度不大.


科目:高中化学 来源: 题型:选择题
| A. | 2×10-10mol/L | B. | $\frac{1}{2}$(10-8+10-10)mol/L | ||
| C. | (10-8+10-10)mol/L | D. | $\frac{1}{2}$(10-6+10-4) |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
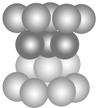
| A. | 此种堆积为面心立方最密堆积 | |
| B. | 该种堆积方式称为铜型 | |
| C. | 该种堆积方式可用符号…ABCABC…表示 | |
| D. | 该种堆积方式所形成晶胞中原子的空间占有率为68% |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | C30H60 | B. | C30H56 | C. | C30H52 | D. | C30H50 |
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com