
依据事实,写出下列反应的热化学方程式。
(1)在25℃、101kPa下,1g甲醇CH3OH(液态)燃烧生成CO2和液态水时放热22.68kJ。则表示甲醇燃烧热的热化学方程式为_________________
(2)若适量的N2和O2完全反应,每生成23克NO2需要吸收16.95kJ热量。________________
(3)用NA表示阿伏加德罗常数,在C2H2(气态)完全燃烧生成CO2和液态水的反应中,每有5NA个电子转移时,放出650kJ的热量。__________________
(4)已知拆开1molH-H键,1molN-H键,1molN≡N键分别需要的能量是436kJ、391kJ、946kJ,则N2与H2反应生成NH3的热化学方程式为___________________
科目:高中化学 来源:2016-2017学年河北省卓越联盟高二上第一次月考化学试卷(解析版) 题型:选择题
已知101 k Pa时辛烷的燃烧热为-5518 kJ· mol-1。则下列热化学方程式书写正确的是( )
A.2C8H18 + 25O2 = 16CO2 + 18H2O △H =-11036 kJ·mol-1
B.2C8H18(l) + 25O2(g) = 16CO2(g) + 18H2O(l) △H =-11036 kJ·mol-1
C.2C8H18(l) + 25O2(g) = 16CO2(g) + 18H2O(g) △H =-11036 kJ·mol-1
D.2C8H18(l) + 25O2(g) = 16CO2(g))+18H2O(l) △H =-5518kJ·mol-1
查看答案和解析>>
科目:高中化学 来源:2017届广东省高三上第二次月考化学试卷(解析版) 题型:实验题
硫代硫酸钠(Na2S2O3•5H2O,式量248)俗名“大苏打”,又称为“海波”,可用于照相业作定型剂,也可用于纸浆漂白作脱氧剂,它易溶于水,难溶于乙醇,加热、遇酸均易分解,工业上常用亚硫酸钠法、硫化碱法等制备,某实验模拟工业硫化碱法制取硫代硫酸钠,其反应装置及所需试剂如图1:
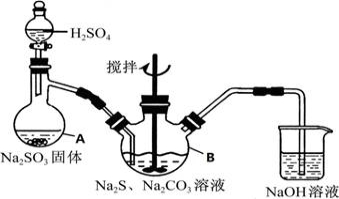
图1
实验具体操作步骤为:
①开启分液漏斗,使硫酸慢慢滴下,适当调节分液漏斗的滴速,使反应产生的SO2气体均匀的通入Na2S和Na2CO3的混合溶液中,同时开启电动搅拌器搅动,水浴加热,微沸
②直至析出的浑浊不再消失,并控制溶液的PH接近7时,停止通入SO2气体
③趁热过滤,将滤液加热浓缩,冷却析出Na2S2O3•5H2O
④在经过滤、洗涤、干燥.得到所需产品
(1)写出仪器A的名称 ,步骤④中洗涤时,为了减少产物的损失的试剂可以
(2)为了保证硫代硫酸钠的产量,实验中不能让溶液PH<7,请用离子方程式解释原因
(3)最后得到的产品可能含有Na2SO4杂质,请设计实验检测产品中是否存在Na2SO4(已知BaS2O3不溶于水),简要说明实验操作.现象和结论
(4)测定产品纯度
①准确称取1.00g产品,用适量蒸馏水溶解,以淀粉作指示剂用0.1000mol•L﹣1碘的标准溶液滴定,反应原理为2S2O32﹣+I2=S4O32﹣+2I﹣,滴定起始和终点的滴定管液面位置如图则消耗碘的标准溶液体积为 mL,产品的纯度为 %
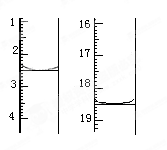
②若滴定时振荡不充分,刚看到溶液局部变色就停止滴定,则会使样品中Na2S2O3•5H2O的质量分数的测量结果________(填“偏高”“偏低”或“不变”)。
(5)Na2S2O3常用于脱氧剂,在溶液中易被Cl2氧化SO42﹣,该反应的离子方程式为. 。
查看答案和解析>>
科目:高中化学 来源:2017届福建省四地六校高三上第一次月考化学试卷(解析版) 题型:选择题
下列条件下,两瓶气体 所含原子数一定相等的是( )
所含原子数一定相等的是( )
A.同质量、不同密度的NO和CO B.同温度、同体积的H2和O2
C.同体积、同密度的C2H4和C3H6 D.同压强、同体积的N2O和CO2
查看答案和解析>>
科目:高中化学 来源:2017届福建省四地六校高三上第一次月考化学试卷(解析版) 题型:选择题
下列离子在给定的条件下一定能大量共存的是( )
A.c(Fe3+)=0.1mol/L的溶液中:NH4+、I-、SO42-、Cl-
B.加入Al粉放出H2的溶液中:Na+、K+、Fe3+、NO3-
C.0. 1 mol·L-1AgNO3溶液:H+、K+、SO42-、Br-
D.pH=12的溶液中:K+、Cl-、CH3COO-、CO32-
查看答案和解析>>
科目:高中化学 来源:2016-2017学年云南省曲靖市高二上第一次月考化学卷(解析版) 题型:选择题
已知在298K时下述反应的有关数据:
C(s)+1/2O2(g)=CO(g) △H1=-110.5kJ/mol
C(s)+O2(g)=CO2(g) △H2=-393.5kJ/mol
则C(s)+CO2(g)=2CO(g)的△H为
A.+283.5kJ/mo B.+ 172.5kJ /mol C.-172.5kJ/mol D.-504 kJ/mol
/mol C.-172.5kJ/mol D.-504 kJ/mol
查看答案和解析>>
科目:高中化学 来源:2016-2017学年四川省高二上10月月考化学试卷(解析版) 题型:填空题
合成氨对化学工业和国防工业具有重要意义。
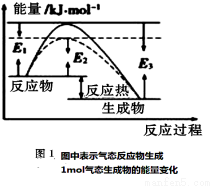

(1)根据图1请写出合成氨的热化学方程式 (热量用E1、E2或E3表示)
(2)向合成塔中按物质的量之比l:4充入N2、H2进行氨的合成,图2为T℃时平衡混合物中氨气的体积分数与压强(p)的关系图。
①图2中氨气的体积分数为15%时,H2的转化率为 。
②图3中T=450℃,则温度为500℃时对应的曲线是 (填“a”或“b”)。
(3)合成氨所需的氢气可由甲烷与水反应制得,反应的热化学方程式为CH4(g)+H2O(g) CO(g)+3H2(g) △H>0,一定温度下,在体积为2 L的恒容容器中发生上述反应,各物质的物质的量变化如下表:
CO(g)+3H2(g) △H>0,一定温度下,在体积为2 L的恒容容器中发生上述反应,各物质的物质的量变化如下表:
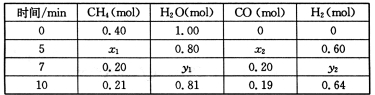
①分析表中数据,判断5 min时反应是否处于平衡状态? (填“是”或“否”),前5 min反应的平均反应速率v(CH4) = 。
②在相同实验条件下,若改为加入CH4 0.1mol,若要求平衡后H2在反应混合气中质量分数不变,则还需加入的物质及其物质的量为
③反应在7~10 min内,CO的物质的量减少的原因可能是 (填字母)。
a.减少CH4的物质的量 b.降低温度 c.升高温度 d.充入H2
④下列方法中可以证明上述已达平衡状态的是
a.单位时间内生成3n mol H2的同时生成n mol CO
b.容器内压强不再变化
c.混合气体密度不再变化
d.混合气体的平均相对分子质量不再变化
e.CH4的质量分数不再变化
⑤已知碳的气化反应在不同温度下平衡常数的对数值(lgK)如下表:

则反应CO(g)+H2O(g)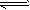 CO2(g)+H2(g)在900K时,该反应平衡常数的对数值(lgK)=_________.
CO2(g)+H2(g)在900K时,该反应平衡常数的对数值(lgK)=_________.
查看答案和解析>>
科目:高中化学 来源:2016-2017学年四川省高二上10月月考化学试卷(解析版) 题型:选择题
一定条件下,通过下列反应可以制备特种陶瓷的原料MgO:
MgSO4(s)+CO(g) MgO(s)+CO2(g)+SO2(g)ΔH>0
MgO(s)+CO2(g)+SO2(g)ΔH>0
该反应在恒容的密闭容器中达到平衡后,若仅改变图中横坐标x的值,重新达到平衡后,纵坐标y随x变化趋势合理的是

选项 | x | y |
A | 温度 | 容器内混合气体的密度 |
B | CO的物质的量 | CO2与CO的物质的量之比 |
C | SO2的浓度 | 平衡常数K |
D | MgSO4的质量(忽略体积) | CO的转化率 |
查看答案和解析>>
科目:高中化学 来源:2016-2017学年广东省高二上第一次大考化学卷(解析版) 题型:选择题
被称之为“软电池”的纸质电池,采用一个薄层纸片作为传导体,在其一边镀锌,而在其另一边镀二氧化锰。在纸内的离子“流过”水和氧化锌组 成的电解液。电池总反应为Zn+2MnO2+H2O=ZnO+2MnO(OH)。下列说法正确的是( )
成的电解液。电池总反应为Zn+2MnO2+H2O=ZnO+2MnO(OH)。下列说法正确的是( )
A.该电池的正极为锌
B.该电池反应中二氧化锰起催化剂作用
C.电池正极反应式为2MnO2+2e-+2H2O=2MnO(OH)+2OH-
D.当0.1molZn完全溶解时,流经电解液的电子个数为1.204×1023
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com