
某同学查资料得知.α-AgI是一种固体导体,导电率很高.固体导体导电的原理是构成离子晶体的某一离子在晶体孔隙中自由移动.他为了研究α-AgI究竟是Ag+导电还是I-导电,设计一个如下图所示(用铅蓄电池做电源)的电化学实验.
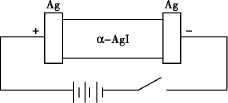
已知铅蓄电池总反应:![]()
(1)铅蓄电池的正极电极方程式:(已知硫酸铅为难溶物)
_____________________________________
(2)若Ag+导电,α-AgI本身质量将________.(填“不变”“变大”或“变小”)
电解池的阳极电极方程式:________
若I-导电,阳极附近的α-AgI晶体密度将会________.(填“不变”“变大”或“变小”)
(3)若通电一段时间后铅蓄电池中消耗了1 mol H2SO4,则电解池的阴极增重________g.
科目:高中化学 来源: 题型:
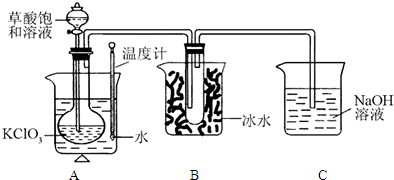
| 实验步骤 | 预期现象和结论 |
| 步骤1: |
|
| 步骤2: |
查看答案和解析>>
科目:高中化学 来源: 题型:阅读理解
| 实验 编号 |
反应温度 (利用水浴加热) |
稀硫酸 溶液 |
MnSO4固体 | 0.10mol/L KMnO4溶液 |
褪色 时间 |
| 1 | 750℃ | ---- | --- | 1mL | 1OOs |
| 2 | 750℃ | 10滴 | ---- | 1mL | 40s |
| 3 | 750℃ | 10滴 | 加入少许 | 1mL | 3s |
| 实验步骤 | 预期现象和结论 |
| 步骤1: |
|
| 步骤2: |
查看答案和解析>>
科目:高中化学 来源:河南省卢氏二高2010届高三上学期期末模拟高三化学试题 题型:038
某同学查资料得知α-AgI是一种固体导体,导电率很高.他为了研究α-AgI究竟是Ag+离子导电还是I-离子导电,设计一个如下图所示(用铅蓄电池做电源)的电化学实验.已知铅蓄电池总反应:
Pb+PbO2+2H2SO4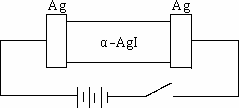
(1)该电解池的阳极电极反应式:________;铅蓄电池的正极电极反应式:________.
(2)若Ag+导电,α-AgI本身质量将________.(填“不变、变大、或变小”)
若I-导电,阳极附近的α-AgI晶体密度将会________.(填“不变、变大、或变小”)
(3)若通电一段时间后铅蓄电池中消耗了1 mol H2SO4,则电解池的阴极增重________g.(不要求写计算过程)
查看答案和解析>>
科目:高中化学 来源:广东省模拟题 题型:实验题


查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com