
| 时间/s | 0 | 1 | 2 | 3 | 4 | 5 |
| c(NO)/mol•L-1 | 1.00 | 0.8 | 0.64 | 0.55 | 0.5 | 0.5 |
| c(CO)/mol•L-1 | 3.50 | 3.30 | 3.14 | 3.05 | 3.00 | 3.00 |

分析 Ⅰ、已知:①2NO(g)+2CO(g)$\stackrel{催化剂}{?}$N2(g)+2CO2(g)△H=a kJ•mol-1,
②2NO(g)+O2(g)═2NO2(g)△H=b kJ•mol-1,
③CO(g)+0.5O2(g)=CO2(g)△H=c kJ•mol-1,
根据盖斯定律①-②+2×③可得2NO2(g)+4CO(g)=N2(g)+4CO2(g);
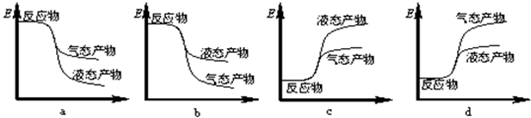
Ⅱ、(1)化学平衡状态的特征(正逆反应速率相等,各组分含量保持不变)判定,C主要图象不符和题设要求,平均摩尔质量应为恒定量;
(2)从表可知2s内NO浓度变化量为0.36mol•L-1,则N2的浓度为0.18mol/L,再有v=$\frac{△c}{△t}$计算;平衡后四种物质平衡浓度为0.5mol•L-1、3mol•L-1、0.25mol•L-1、0.5mol•L-1,根据化学平衡常数概念列式计算;
(3)①根据水解平衡常数Kh=$\frac{c(N{H}_{3}•{H}_{2}O)c({H}^{+})}{c(N{{H}_{4}}^{+})}$=$\frac{c(N{H}_{3}•{H}_{2}O)c({H}^{+})}{c(N{{H}_{4}}^{+})}•\frac{c(O{H}^{-})}{c(O{H}^{-})}$=$\frac{{K}_{w}}{{K}_{b}}$计算;
②在(NH4)2SO4溶液中存在水解反应,2NH4++H2O?NH3•H2O+H+,往(NH4)2SO4溶液中再加入少量 (NH4)2SO4固体,水解平衡向正方向进行,但铵根的水解率减小,可得;
(4)①原电池的正极判断根据N元素化合价变化情况判断,氮元素化合价降低在正极发生;
②负极失电子被氧化:CO+O2--2e-=CO2;
Ⅲ、如图2所示,无摩擦、无质量的活塞1、2将反应器隔成甲、乙两部分,说明为等压容器,对应2CO(g)+2NO(g)?N2(g)+2CO2(g)只要转化到一边成比例即等效,若去掉活塞1,不引起活塞2的移动,说明新平衡与原平衡等效,据此分析;
解答 解:Ⅰ、已知①2NO(g)+2CO(g)$\stackrel{催化剂}{?}$N2(g)+2CO2(g)△H=a kJ•mol-1
②2NO(g)+O2(g)=2NO2(g)△H=b kJ•mol-1;
③CO(g)+0.5O2(g)=CO2(g)△H=c kJ•mol-1
根据盖斯定律①-②+2×③可得2NO2(g)+4CO(g)=N2(g)+4CO2(g))△H=a-b+2c kJ•mol-1;
故答案为:2NO2(g)+4CO(g)=N2(g)+4CO2(g)△H=a-b+2c kJ•mol-1;
Ⅱ、(1)A、随着反应的进行,氮气的百分量瞪大,平衡时不再变化,故A正确;
B、△H与反应的物质的量有关,故△H改变,与图象不符,故B错误;
C、混合我替的总质量不变,该反应的混合气体的总的物质的量变小,根据$\overline{M}=\frac{m}{n}$,平均相对分子质量增大,平衡时不再改变,故C错误;
D、CO作为反应物,随着反应的进行,浓度减小,平衡时保持不变,故D正确;
故选AD;
(2)从表可知2s内NO浓度变化量为0.36mol•L-1,则N2的浓度为0.18mol/L,故其速率为$\frac{0.18mol/L}{2s}$=0.09mol•L-1•min-1;平衡后四种物质平衡浓度为0.5mol•L-1、3mol•L-1、0.25mol•L-1、0.5mol•L-1,故平衡常数K=$\frac{0.{5}^{2}×0.25}{0.5×{3}^{2}}$=0.03mol•L-1;
故答案为:0.09; 0.03mol•L-1;
(3)①水解平衡常数Kh=$\frac{c(N{H}_{3}•{H}_{2}O)c({H}^{+})}{c(N{{H}_{4}}^{+})}$=$\frac{c(N{H}_{3}•{H}_{2}O)c({H}^{+})}{c(N{{H}_{4}}^{+})}•\frac{c(O{H}^{-})}{c(O{H}^{-})}$=$\frac{Kw}{Kb}$,pH=5,c(H+)=1×10-5,则$\frac{c(N{{H}_{4}}^{+})}{c(N{H}_{3}•{H}_{2}O)}$=$\frac{c({H}^{+})}{Kh}$=$\frac{c({H}^{+})Kb}{Kw}$=$1{0}^{-5}×\frac{1.7×1{0}^{-5}}{1×1{0}^{-14}}$=1.7×104;
故答案为:1.7×104;
②在(NH4)2SO4溶液中存在水解反应,2NH4++H2O?NH3•H2O+H+,往(NH4)2SO4溶液中再加入少量 (NH4)2SO4固体,水解平衡向正方向进行,但铵根的水解率减小,所以$\frac{c(N{{H}_{4}}^{+})}{c(S{{O}_{4}}^{2-})}$的值将变大;
故答案为:变大;
(4)①氮元素化合价降低在正极发生,pt电极为正极;
②负极失电子被氧化,CO氧化为CO2,负极电极式为:CO+O2--2e-=CO2;
故答案为:正极;CO+O2--2e-=CO2;
Ⅲ、如图2所示,无摩擦、无质量的活塞1、2将反应器隔成甲、乙两部分,说明为等压容器,对应2CO(g)+2NO(g)?N2(g)+2CO2(g)只要转化到一边成比例即等效,所以有
2CO(g)+2NO(g)?N2(g)+2CO2(g);
甲起始(mol):0.6 0 x 3
转化(mol):0.6+2x 2x 0 3-2x
乙起始(mol):1.2 1 0 0
若去掉活塞1,不引起活塞2的移动,说明新平衡与原平衡等效,则3-2x=0,解得x=1.5mol,
则甲相等于3.6molCO和3molNO刚好是乙的3倍,所以V甲:V乙=3:1;
故答案为:1.5;3:1.
点评 本题考查了热化学方程式书写、速率计算、平衡常数计算、盐类水解、原电池工作原理及电极反应书写、等效平衡,综合性强,要求学生对基础知识的掌握扎实,计算较大,(3)、Ⅲ题目难度大.


 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案科目:高中化学 来源: 题型:解答题
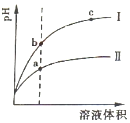 常温下有0.1mol•L-1四种溶液NaOH、NH3•H2O、HCl、CH3COOH
常温下有0.1mol•L-1四种溶液NaOH、NH3•H2O、HCl、CH3COOH查看答案和解析>>
科目:高中化学 来源: 题型:解答题
 降低大气中CO2的含量及有效地开发利用 CO2,目前工业上有一种方法是用CO2来生产燃料甲醇.为探究反应原理,现进行如下实验,在体积为1L的恒容密闭容器中,充入1mol CO2和3mol H2,一定条件下发生反应:CO2(g)+3H2(g)?CH3OH(g)+H2O(g)△H=-49.0kJ/mol.测得CO2和CH3OH(g)的浓度随时间变化如图所示.
降低大气中CO2的含量及有效地开发利用 CO2,目前工业上有一种方法是用CO2来生产燃料甲醇.为探究反应原理,现进行如下实验,在体积为1L的恒容密闭容器中,充入1mol CO2和3mol H2,一定条件下发生反应:CO2(g)+3H2(g)?CH3OH(g)+H2O(g)△H=-49.0kJ/mol.测得CO2和CH3OH(g)的浓度随时间变化如图所示.查看答案和解析>>
科目:高中化学 来源: 题型:实验题
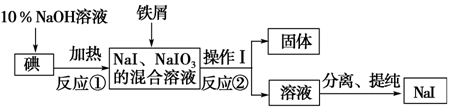
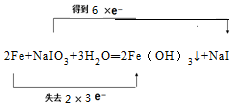 .
.查看答案和解析>>
科目:高中化学 来源: 题型:解答题
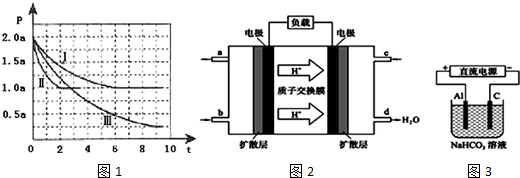
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
| t/s | 0 | 500s | 1 000s |
| c(H2)/(mol•L-1) | 5.00 | 3.52 | 2.48 |
| c(CO)/(mol•L-1) | 2.50 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
| 2min | 4min | 6min | 8min | … | |
| CO | 0.07 | 0.06 | 0.06 | 0.05 | … |
| H2 | x | 0.12 | 0.12 | 0.2 | … |
| CH3OH | 0.03 | 0.04 | 0.04 | 0.05 | … |
查看答案和解析>>
科目:高中化学 来源: 题型:实验题

查看答案和解析>>
科目:高中化学 来源: 题型:解答题
 CO是火力发电厂释放出的主要尾气,为减少对环境污染,发电厂试图采用CO与Cl2在催化剂的作用下合成光气(COCl2).某温度下,向2L的密闭容器中投入一定量的CO和Cl2,在催化剂的作用下发生反应:CO(g)+Cl2(g)?COCl2(g)△H=a kJ/mol
CO是火力发电厂释放出的主要尾气,为减少对环境污染,发电厂试图采用CO与Cl2在催化剂的作用下合成光气(COCl2).某温度下,向2L的密闭容器中投入一定量的CO和Cl2,在催化剂的作用下发生反应:CO(g)+Cl2(g)?COCl2(g)△H=a kJ/mol| t/min | n (CO)/mol | n (Cl2)/mol |
| 0 | 1.20 | 0.60 |
| 1 | 0.90 | |
| 2 | 0.80 | |
| 4 | 0.20 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com