
 =0.00100mol,
=0.00100mol,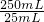 =0.01mol,
=0.01mol,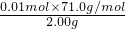 ×100%=35.5%,
×100%=35.5%,

 名师伴你成长课时同步学练测系列答案
名师伴你成长课时同步学练测系列答案科目:高中化学 来源: 题型:
工业上常用漂白粉跟酸反应放出的氯气的质量分数x%来表示漂白粉的优劣。漂白粉与酸反应为:Ca(ClO)2+CaCl2+2H2SO4=2CaSO4+2H2O+2Cl2↑,又知I2与Na2S2O3溶液反应为I2+2Na2S2O3=Na2S4O6+2NaI。
现为了测定一瓶漂白粉的x%,进行了如下实验。称取漂白粉样品2.00g,加水研磨后,转入250mL容量瓶内,用水稀释至刻度。摇匀后,取出25.0mL,加入过量的KI溶液和过量的稀H2SO4,静置。待漂白粉放出的氯气与KI完全反应后,用0.100mol/L Na2S2O3溶液20.0mL。试由上述数据计算该漂白粉的x%。
查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
Ca(ClO)2+CaCl2+2H2SO4=2CaSO4+2Cl2↑+2H2O
现为了测定一瓶漂白粉的x%,进行了如下实验。称取漂白粉样品2.
2Na2S2O3+I2=Na2S4O6+2NaI
滴定时用去Na2S2O3溶液20.0mL。试由上述数据计算该漂白粉的x%。
查看答案和解析>>
科目:高中化学 来源: 题型:
工业上常用漂白粉跟酸反应制得的氯气对漂白粉的质量分数(x%)来表示漂白粉的优劣。现为测定一瓶漂白粉的x%,进行如下实验:称取漂白粉样品2.00g,加水研磨后转入250mL容量瓶内,用水稀释至刻度。摇匀后,取出25.0mL,加入过量的KI溶液和过量的稀硫酸,静置待漂白粉放出的氯气与KI完全反应后,加入0.100mol?L-1的Na2S2O3溶液20.00mL,恰好与生成的碘完全反应:
2Na2S2O3+I2=Na2S4O6+2NaI
(1)试写出漂白粉与稀硫酸反应的化学方程式 。
(2)试由上述数据计算该漂白粉的x%为 。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com