
镁和铝的混合物12.6 g,放入100 mL某浓度的氢氧化钠溶液中充分反应,生成气体3.36 L(标准状况),再向其中加入足量盐酸,固体完全反应后又生成气体10.08 L(标准状况),求:
(1)氢氧化钠溶液的物质的量浓度.
(2)原混合物中镁、铝的质量各为多少克.
 通城学典默写能手系列答案
通城学典默写能手系列答案 金牌教辅培优优选卷期末冲刺100分系列答案
金牌教辅培优优选卷期末冲刺100分系列答案科目:高中化学 来源:山东省济南外国语学校2009-2010学年高一下学期3月质检化学试题 题型:022
(1)铝是一种重要的金属材料,铝热反应可以焊接钢轨,请写出铝在高温下与三氧化二铁反应的化学方程式___________.
(2)铝合金中含有合金元素镁、铜、硅,为了测定合金中铝的含量,设计了如下实验,请回答有关问题:
①称取样品a g,将样品溶于足量的稀盐酸,过滤.
②滤液中加入过量的氢氧化钠溶液,过滤.有关的离子方程式为________
③步骤②的滤液中通过足量的CO2气体,可产生Al(OH)3沉淀,过滤.
④步骤③过滤后的滤渣用蒸馏水洗涤数次,烘干并灼烧至恒重,冷却后称量,其质量为b g,原样品中铝的质量分数为________.
(3)计算机的芯片、化学实验室的玻璃仪器都是以硅或硅的化合物为材料制成的,但盛放NaOH溶液的试剂瓶不能用玻璃塞,原因是(写反应的离子方程式)________;工业上,硅是在电炉中用炭粉还原二氧化硅制得的,写出该反应的化学方程式________,若往电炉中加入12 g二氧化硅和足量炭粉的混合物,生成的气体在标准状况下的体积为________.
查看答案和解析>>
科目:高中化学 来源:上海市奉贤区2013年高考一模化学试题 题型:058
镁、铝、铁及其化合物在生产和生活中有广泛的应用.
1.镁铝合金用在飞机制造业,现有3.90克镁铝合金溶于足量的2 mol/L稀硫酸中生成0.2 mol氢气,计算并确定镁铝合金中物质的量n(Mg)∶n(Al)=________.
2.硫铁矿的主要成分为FeS2(假设杂质只含SiO2)是生产硫酸的原料.取某硫铁矿10 g在足量的空气中煅烧(4FeS2+11O2→2Fe2O3+8SO2),充分反应后冷却,称得固体质量为7.4 g(杂质SiO2不反应).该硫铁矿中FeS2的质量分数为________.
3.现有一定量的铁粉和铝粉组成的混合物跟100 mL稀硝酸充分反应,反应过程中无任何气体放出,往反应后的澄清溶液中逐渐加入4.00 mol·L-1的NaOH溶液,加入NaOH溶液的体积与产生沉淀的质量的关系如图所示(必要时可加热,忽略气体在水中的溶解):纵坐标中A点的数值是________.

4.炼铁厂生产的生铁常用于炼钢.取某钢样粉末28.12 g(假设只含Fe和C),在氧气流中充分反应,得到CO2气体224 mL(标准状况下).
(1)计算此钢样粉末中铁和碳的物质的量之比为________(最简单的整数比).
(2)再取三份不同质量的上述钢样粉末分别加到100 mL相同浓度的稀H2SO4中,充分反应后,测得的实验数据如下表所示:
则该硫酸溶液的物质的量浓度为________.
(3)若在上述实验Ⅱ中继续加入m克钢样粉末,计算反应结束后剩余的固体质量为________g.(保留3位小数)
查看答案和解析>>
科目:高中化学 来源:2012届山东省曲阜师大附中高三9月教学质量检测化学试卷 题型:填空题
( 12 分)(1)某校化学兴趣小组用如下图所示过程除去AlCl3中含有的Mg2+、K+杂质离子并尽可能减少AlCl3的损失。请回答下列问题:
①写出混合物中加入足量氢氧化钠溶液时,溶液中发生反应的离子方程式:
。
②溶液a中存在的阴离子有__________________;在溶液a中加入盐酸时需控制溶液的pH的原因是_______________________________________;为此,改进方法是 。
?(2)?该化学小组又测定一定质量的某镁铝混合物中镁的质量分数,设计了如下实验方案:
方案Ⅰ:镁铝混合物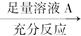 测定生成气体的体积
测定生成气体的体积
方案Ⅱ:镁铝混合物 测定剩余固体的质量
测定剩余固体的质量
下列有关判断中不正确的是 ?(填代号)
| A.溶液A选用NaOH溶液 |
| B.若溶液B选用浓硝酸,则测得镁的质量分数偏小 |
| C.溶液A和B均可选用稀硝酸 |
| D.实验室中方案Ⅱ更便于实施 |
查看答案和解析>>
科目:高中化学 来源:2011-2012学年山东省高三9月教学质量检测化学试卷 题型:填空题
( 12 分)(1)某校化学兴趣小组用如下图所示过程除去AlCl3中含有的Mg2+、K+杂质离子并尽可能减少AlCl3的损失。请回答下列问题:

①写出混合物中加入足量氢氧化钠溶液时,溶液中发生反应的离子方程式:
。
②溶液a中存在的阴离子有__________________;在溶液a中加入盐酸时需控制溶液的pH的原因是_______________________________________;为此,改进方法是 。
(2)该化学小组又测定一定质量的某镁铝混合物中镁的质量分数,设计了如下实验方案:
方案Ⅰ:镁铝混合物 测定生成气体的体积
测定生成气体的体积
方案Ⅱ:镁铝混合物 测定剩余固体的质量
测定剩余固体的质量
下列有关判断中不正确的是 (填代号)
A.溶液A选用NaOH溶液
B.若溶液B选用浓硝酸,则测得镁的质量分数偏小
C.溶液A和B均可选用稀硝酸
D.实验室中方案Ⅱ更便于实施
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com