
利用NO2平衡气体遇热颜色加深、遇冷颜色变浅来指示放热过程和吸热过程。

①按图所示将实验装置连接好。
②向甲烧杯的水中投入一定量的CaO固体,此烧杯中的NO2平衡混合气体的红棕色变深;向乙烧杯中加入NH4NO3晶体,此时烧杯中NO2平衡混合气体颜色变浅。回答下列问题:
(1)CaO与水反应的化学方程式为 _,
该反应为________ __ _ _(填“吸热反应”或“放热反应”)。
(2)NH4NO3晶体溶于水温度________(填“升高”或“降低”);NH4NO3溶于水_____ ______ (填“是”或“不是”)吸热反应。
(3)查阅资料知NO2的平衡气体中存在的可逆反应为2NO2(g) N2O4(g),已知NO2为红棕色,N2O4为无色,结合实验知,当温度升高时,平衡__ _ _____(填“未被破坏”或“发生移动”),此时反应速率________(填“增大”、“减小”或“不变化”)。混合气体的颜色不变______(填“能”或“不能”)证明反应已达平衡。
N2O4(g),已知NO2为红棕色,N2O4为无色,结合实验知,当温度升高时,平衡__ _ _____(填“未被破坏”或“发生移动”),此时反应速率________(填“增大”、“减小”或“不变化”)。混合气体的颜色不变______(填“能”或“不能”)证明反应已达平衡。
 举一反三同步巧讲精练系列答案
举一反三同步巧讲精练系列答案 口算与应用题卡系列答案
口算与应用题卡系列答案 名师点睛字词句段篇系列答案
名师点睛字词句段篇系列答案科目:高中化学 来源: 题型:
A、B、C均为短周期元素,A、B同周期,A、C的最低价阴离子分别为A2-、C-,A2-离子半径大于C-,B2+与C-具有相同的电子层结构。下列叙述中一定不正确的是( )
A. 它们的原子序数A>B>C B. 它们的原子半径C>B>A
C. 它们的离子半径A2->C->B2+ D. 它们的最外层电子数C>A>B
查看答案和解析>>
科目:高中化学 来源: 题型:
三氟化氮(NF3)是微电子工业中一种优良的等离子刻蚀气体,它在潮湿的环境中能发生反应:3NF3+5H2O===2NO+HNO3+9HF,下列有关该反应的说法正确的是 ( )
A.NF3是氧化剂,H2O是还原剂
B.HF是还原产物
C.还原剂和氧化剂的物质的量之比是2∶1
D.NF3在潮湿的空气中泄漏会产生红棕色气体
查看答案和解析>>
科目:高中化学 来源: 题型:
如图所示是Zn和Cu形成的原电池,某实验兴趣小组做完实验后,在读书卡上的记录如下,则卡片上描述合理的是( )。
①Cu为负极,Zn为正极
②Cu极上有气泡产生,发生还原反应
③SO42- 向Cu极移动
④若有0.5 mol电子流经导线,则可产生0.25 mol气体
⑤电子的流向是:Cu―→Zn
⑥正极反应式:Cu+2e-===Cu2+,发生氧化反应
A.①②③ B.②④⑥ C.③④⑤ D.②④
查看答案和解析>>
科目:高中化学 来源: 题型:
研究人员最近发现了一种“水电池”,这种电池能利用淡水与海水之间含盐量的差别进行发电,在海水中电池总反应式为:5MnO2+2Ag+2NaCl=Na2Mn5O10+2AgCl,下列对“水电池”在海水中放电时的有关说法正确的是( )
A.正极反应式为:5MnO2+2e-= Mn5O102- B.每生成1mol AgCl转移2mol电子
C.Cl-不断向“水电池”的正极移动 D.Ag发生还原反应
查看答案和解析>>
科目:高中化学 来源: 题型:
下列关于浓硫酸和浓硝酸的叙述正确的是( )。
A.浓硫酸具有吸水性,因而能使蔗糖炭化
B.久置的浓硝酸会发黄,是因为HNO3不稳定,分解产生NO2溶于其中
C.常温下,浓硫酸和浓硝酸均可以与铜反应,放出气体
D.常温下可用铁制容器运输浓硫酸和浓硝酸,是因为它们与铁不反应
查看答案和解析>>
科目:高中化学 来源: 题型:
下列离子在指定溶液中能大量共存的是( )。
①pH=11的溶液中:CO3 2-、Na+、AlO2-、NO3-;②无色透明溶液中:K+、Na+、MnO4-、SO42- ;③含有大量Fe3+的溶液中:NH4+、Na+、Cl-、SCN-;④酸性溶液中:Fe2+、Al3+、NO3-、Cl-;⑤使酚酞试液呈红色的溶液中:K+、CO32-、NO3-、SO42- 。
A.①⑤ B.②③ C.①④ D.③⑤
查看答案和解析>>
科目:高中化学 来源: 题型:
某可充电的锂离子电池以LiMn2O4为正极,嵌入锂的碳材料为负极,含Li+导电固体为电解质。放电时的电池反应为:Li+LiMn2O4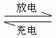 Li2Mn2O4。下列说法正确的是 ( )
Li2Mn2O4。下列说法正确的是 ( )
A.放电时,LiMn2O4发生氧化反应
B.放电时,正极反应为:Li++LiMn2O4+e-==Li2Mn2O4
C.充电时,LiMn2O4发生氧化反应
D.充电时,阳极反应为:Li++e-==Li
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com