
| A. | NH3的电子式: | |
| B. | 氯离子的结构示意图: | |
| C. | CS2的结构式:S=C=S | |
| D. | 原子核内有10个中子的氧原子:${\;}_{8}^{18}$O |
分析 A.N原子最外层5个电子;
B.氯离子的核电荷数为17,不是18;
C.CS2的电子式类似于CO2,二者都为分子晶体;
D.原子符号zAX左下角z代表质子数,左上角A代表质量数,X代表元素符号,质量数=质子数+中子数.
解答 解:A.氨气是共价化合物,各原子间通过共用电子对形成共价键,所以其电子式为: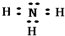 ,故A错误;
,故A错误;
B.氯离子的核电荷数为17,核外电子总数为18,其正确的离子结构示意图为: ,故B正确;
,故B正确;
C.CS2的电子式类似于CO2,电子式为 ,结构式为:S=C=S,故C正确;
,结构式为:S=C=S,故C正确;
D.氧元素的质子数为8,原子核内有10个中子的氧原子,中子数为8+10=10,该原子的原子符号为818O,故D正确.
故选A.
点评 本题考查常用化学用语书写判断,题目难度中等,掌握常用化学用语的书写原则为解答关键,注意结构式未成键的孤对电子对不用标出,为易错点.


科目:高中化学 来源: 题型:填空题

查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 蒸馏实验中,为了防止暴沸,要在蒸馏烧瓶中加入沸石 | |
| B. | 可用丁达尔效应区别溶液和胶体 | |
| C. | 用CCl4萃取碘水后分液时,先打开分液漏斗活塞,放出下层液体,再关闭活塞,从漏斗上口倒出上层液体 | |
| D. | 检验某溶液中是否含有Fe2+时,可先加入适量的氯水,再滴加硫氰化钾溶液,若溶液变为红色,则说明溶液中一定含有Fe2+ |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | ①④ | B. | ②⑥ | C. | ③⑤ | D. | ②⑤ |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 肯定不含I- | B. | 肯定不含NH4+ | C. | 可能含有SO32- | D. | 可能含有I- |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 水玻璃中通人过量二氧化碳:Na2SiO3+CO2+H2═2Na++CO${\;}_{3}^{2-}$+H2SiO3 | |
| B. | Na202加入H2180中:2Na2O2+2H${\;}_{2}^{18}$O═4Na++4OH-+${\;}_{\;}^{18}$O2↑ | |
| C. | 硅与氢氟酸的反应:Si+4H++4F-═SiF4↑+2H2↑ | |
| D. | 过量C02通入氢氧化钙溶液中:CO2+OH-═HCO${\;}_{3}^{-}$ |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 质子数27的钴-60原子:60 27Co | |
| B. | 氯化铵的电子式: | |
| C. | S2-的结构示意图: | |
| D. | Cl-的电子排布式:1s22s22p63s23p5 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com