
氮是地球上含量最丰富的一种元素,氮及其化合物在工农业生产、生活中有着重要作用。请回答下列问题:
(1)右图是1 mol NO2和1mol
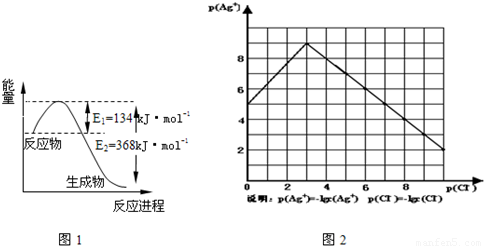
CO反应生成CO2和NO过程中能量变化示意图,请写出NO2和CO反应的热化学方程式
。
(2)在0.5L的密闭容器中,一定量的氮气和氢气进行如下化学反应:N2(g)+3H2(g)
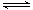 2NH3(g)△H<0其化学平衡常数K与温度t的关系如右表:请完成下列问题;
2NH3(g)△H<0其化学平衡常数K与温度t的关系如右表:请完成下列问题;
|
t/℃ |
200 |
300 |
400 |
|
K |
K1 |
K2 |
0.5 |
①试比较K1、K2的大小,K1____K2(填写“>”、“=”或“<”)
②下列各项能作为判断该反应达到化学平衡状态的依据是____一(填序号字母)
a.容器内N2、H2、NH3的浓度之比为1:3:2
b.v(N2)正=3v(H2)逆
c.容器内压强保持不变
d.混合气体的密度保持不变
③400℃时,反应2NH3(g) 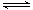 N2(g)+3H2(g)的化学平衡常数的值为 。当测得NH3和N2、H2的物质的量分别为3mol和2mol、1mol时,则该反应的v(N2)正 __
v(N2)逆(填写“>”、“=”或“<”=)
N2(g)+3H2(g)的化学平衡常数的值为 。当测得NH3和N2、H2的物质的量分别为3mol和2mol、1mol时,则该反应的v(N2)正 __
v(N2)逆(填写“>”、“=”或“<”=)
(1)NO2(g)+CO(g)  CO2(g)+NO(g);△H=-234kJ/mol (2) ①
> ② c ③ 2 >
CO2(g)+NO(g);△H=-234kJ/mol (2) ①
> ② c ③ 2 >
【解析】
试题分析:(1)由图可知:NO2和CO反应的热化学方程式为:NO2(g)+CO(g)  CO2(g)+NO(g);△H=-234kJ/mol 。(2)
①升高温度化学平衡向吸热反应方向移动。由于该反应的正反应是放热反应。所以升高温度化学平衡向逆反应方向移动。平衡越向逆反应方向移动,反应的平衡常数就越小。所以K1 >K2。②a平衡时各物质的浓度与起始加入的物质的多少有关。只要平衡时各种物质的浓度不变,反应就达到了平衡。错误。b.在任何时刻都有3v(N2)正=v(H2)正,而v(N2)正=3v(H2)逆,代入第一个式子可得9 v(H2)逆= v(H2)正。由于V(H2)正>V(H2)逆。反应未达到平衡。错误。c.由于容器的容积不变,若反应达到平衡,各种物质的物质的量不变,容器内压强也保持不变 。正确。 d.反应无论进行到什么程度,质量都不会发生变化,那么任何时刻混合气体的密度都保持不变。所以不能根据容器的容积不变来判断反应达到平衡。错误。选项为:C. ③400℃时,2NH3(g)
CO2(g)+NO(g);△H=-234kJ/mol 。(2)
①升高温度化学平衡向吸热反应方向移动。由于该反应的正反应是放热反应。所以升高温度化学平衡向逆反应方向移动。平衡越向逆反应方向移动,反应的平衡常数就越小。所以K1 >K2。②a平衡时各物质的浓度与起始加入的物质的多少有关。只要平衡时各种物质的浓度不变,反应就达到了平衡。错误。b.在任何时刻都有3v(N2)正=v(H2)正,而v(N2)正=3v(H2)逆,代入第一个式子可得9 v(H2)逆= v(H2)正。由于V(H2)正>V(H2)逆。反应未达到平衡。错误。c.由于容器的容积不变,若反应达到平衡,各种物质的物质的量不变,容器内压强也保持不变 。正确。 d.反应无论进行到什么程度,质量都不会发生变化,那么任何时刻混合气体的密度都保持不变。所以不能根据容器的容积不变来判断反应达到平衡。错误。选项为:C. ③400℃时,2NH3(g)  N2(g)+3H2(g)的化学平衡常数和反应N2(g)+3H2(g)
N2(g)+3H2(g)的化学平衡常数和反应N2(g)+3H2(g)  2NH3(g)的化学平衡常数互为倒数。即为2,。由于C2(NH3)/C(N2)C3(H2)=62/(4×23)=9/8<2.所以反应向正反应方向移动。即V(N2)正> V(N2)逆。
2NH3(g)的化学平衡常数互为倒数。即为2,。由于C2(NH3)/C(N2)C3(H2)=62/(4×23)=9/8<2.所以反应向正反应方向移动。即V(N2)正> V(N2)逆。
考点:考查热化学方程式的书写及平衡状态的判断等知识。


 阅读快车系列答案
阅读快车系列答案科目:高中化学 来源: 题型:阅读理解
 I.描述弱电解质电离情况可以用电离度和电离平衡常数表示,下表1是常温下几种弱酸的电离平衡常数(Ka)和弱碱的电离平衡常数(Kb).
I.描述弱电解质电离情况可以用电离度和电离平衡常数表示,下表1是常温下几种弱酸的电离平衡常数(Ka)和弱碱的电离平衡常数(Kb).| 酸或碱 | 电离平衡常数(Ka或 Kb) |
| CH3COOH | 1.8×10-5 |
| HNO2 | 4.6×10-4 |
| HCN | 5×10-10 |
| HClO | 3×10-8 |
| NH3?H2O | 1.8×10-5 |
| t/℃ | 200 | 300 | 400 |
| K | K1 | K2 | 0.5 |
查看答案和解析>>
科目:高中化学 来源: 题型:阅读理解
| t/℃ | 200 | 300 | 400 |
| K | K1 | K2 | 0.5 |
查看答案和解析>>
科目:高中化学 来源: 题型:阅读理解
I.描述弱电解质电离情况可以用电离度和电离平衡常数表示,下表1是常温下几种弱酸的电离平衡常数(Ka)和弱碱的电离平衡常数(Kb)。表1
| 酸或碱 | 电离平衡常数(Ka或 Kb) |
| CH3COOH | 1.8×10-5 |
| HNO2 | 4.6×10-4 |
| HCN | 5×10-10 |
| HClO | 3×10-8 |
| NH3·H2O | 1.8×10-5 |
请回答下列问题:
(1)上述四种酸中,酸性最弱的是 (用化学式表示)。下列能使醋酸溶液中CH3COOH的电离程度增大,而电离平衡常数不变的操作是 (填序号)。
A.升高温度 B.加水稀释 C.加少量的CH3COONa固体 D.加少量冰醋酸
(2)CH3COONH4的水溶液呈 (选填“酸性”“中性”或“碱性”),理由是:
,
溶液中各离子浓度大小的关系是 。
II.氮是地球上含量最丰富的一种元素,氮及其化合物在工农业生产、生活中有着重要作用。请回答下列问题:(图中涉及物质为气态)

(1)上图是1 mol NO2和1mol CO反应生成CO2和NO过程中能量变化示意图,请写出NO2和CO反应的热化学方程式 。
(2)在0.5L的密闭容器中,一定量的氮气和氢气进行如下化学反应:
N2(g)+3H2(g)![]() 2NH3(g)△H<0,其化学平衡常数K与温度t的关系如下表:请完成下列问题。
2NH3(g)△H<0,其化学平衡常数K与温度t的关系如下表:请完成下列问题。
| t/℃ | 200 | 300 | 400 |
| K | K1 | K2 | 0.5 |
①试比较K1、K2的大小,K1_ K2(填写“>”、“=”或“<”)。
②下列各项能作为判断该反应达到化学平衡状态的依据是____(填序号字母):
a.容器内N2、H2、NH3的浓度之比为1:3:2 b.v(N2)正=3v(H2)逆
c.容器内压强保持不变 d.混合气体的密度保持不变
③在400℃时, 当测得NH3和N2、H2的物质的量分别为1mol和2mol、3mol时,则该反应的v(N2)正_ _ v(N2)逆(填写“>”、“=”或“<”)
查看答案和解析>>
科目:高中化学 来源: 题型:阅读理解
I.描述弱电解质电离情况可以用电离度和电离平衡常数表示,下表1是常温下几种弱酸的电离平衡常数(Ka)和弱碱的电离平衡常数(Kb)。表1
| 酸或碱 | 电离平衡常数(Ka或 Kb) |
| CH3COOH | 1.8×10-5 |
| HNO2 | 4.6×10-4 |
| HCN | 5×10-10 |
| HClO | 3×10-8 |
| NH3·H2O | 1.8×10-5 |
请回答下列问题:
(1)上述四种酸中,酸性最弱的是 (用化学式表示)。下列能使醋酸溶液中CH3COOH的电离程度增大,而电离平衡常数不变的操作是 (填序号)。
A.升高温度 B.加水稀释 C.加少量的CH3COONa固体 D.加少量冰醋酸
(2)CH3COONH4的水溶液呈 (选填“酸性”“中性”或“碱性”),理由是:
,
溶液中各离子浓度大小的关系是 。
II.氮是地球上含量最丰富的一种元素,氮及其化合物在工农业生产、生活中有着重要作用。请回答下列问题:(图中涉及物质为气态)

(1)上图是1 mol NO2和1mol CO反应生成CO2和NO过程中能量变化示意图,请写出NO2和CO反应的热化学方程式 。
(2)在0.5L的密闭容器中,一定量的氮气和氢气进行如下化学反应:
N2(g)+3H2(g)![]() 2NH3(g)△H<0,其化学平衡常数K与温度t的关系如下表:请完成下列问题。
2NH3(g)△H<0,其化学平衡常数K与温度t的关系如下表:请完成下列问题。
| t/℃ | 200 | 300 | 400 |
| K | K1 | K2 | 0.5 |
①试比较K1、K2的大小,K1_ K2(填写“>”、“=”或“<”)。
②下列各项能作为判断该反应达到化学平衡状态的依据是____(填序号字母):
a.容器内N2、H2、NH3的浓度之比为1:3:2 b.v(N2)正=3v(H2)逆
c.容器内压强保持不变 d.混合气体的密度保持不变
③在400℃时, 当测得NH3和N2、H2的物质的量分别为1mol和2mol、3mol时,则该反应的v(N2)正_ _ v(N2)逆(填写“>”、“=”或“<”)
查看答案和解析>>
科目:高中化学 来源:2013届黑龙江省大庆铁人中学高三第三次阶段化学试卷(带解析) 题型:填空题
(12分)I.描述弱电解质电离情况可以用电离度和电离平衡常数表示,下表1是常温下几种弱酸的电离平衡常数(Ka)和弱碱的电离平衡常数(Kb)。表1
| 酸或碱 | 电离平衡常数(Ka或 Kb) |
| CH3COOH | 1.8×10-5 |
| HNO2 | 4.6×10-4 |
| HCN | 5×10-10 |
| HClO | 3×10-8 |
| NH3·H2O | 1.8×10-5 |

 2NH3(g)△H<0,其化学平衡常数K与温度t的关系如下表:请完成下列问题。
2NH3(g)△H<0,其化学平衡常数K与温度t的关系如下表:请完成下列问题。| t/℃ | 200 | 300 | 400 |
| K | K1 | K2 | 0.5 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com