
| A. | 甲烷是含碳量最低的碳氢化合物 | |
| B. | 所有的碳氢化合物分子组成均符合Cn H2n+2的通式 | |
| C. | 碳氢化合物一般都不溶于水 | |
| D. | 碳氢化合物分子中的化学键一定有极性键,也可能有非极性键 |
分析 A、根据碳的四价结构,可知1个碳原子最多与4个H原子结合;
B、只有烷烃的分子组成通式符合CnH2n+2;
C、烃都不溶于水;
D、烃分子中一定存在C-H,由不同原子形成的共价键,为极性键,分子中碳原子数目大于1时,会存在碳碳之间形成的共价键,会存在非极性键.
解答 解:A、根据碳的四价结构,可知1个碳原子最多与4个H原子结合,所以甲烷是含碳量最低的碳氢化合物,故A正确;
B、只有烷烃的分子组成通式符合CnH2n+2,烯烃分子组成通式为CnH2n+2,炔烃分子组成通式为CnH2n-2,故B错误;
C、所有的烃都不溶于水,故C正确;
D、烃分子中一定存在C-H,为极性键,烃分子存在碳碳之间形成的共价键,会存在非极性键,如乙烯中碳碳双键,乙炔中碳碳三键,故D正确.
故选:B.
点评 本题主要考查烃的结构与性质,难度不大,注意基础知识的积累与掌握.


科目:高中化学 来源: 题型:解答题
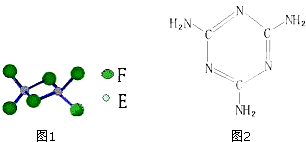
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 碳元素 | B. | 氢元素 | C. | 氧元素 | D. | 氢、氧元素 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 浓硝酸与足量铜片反应时,先生成红棕色气体,后生成无色气体 | |
| B. | 氧化铝的熔点很高,可用于制造熔融烧碱的坩埚 | |
| C. | 在含FeC12杂质的FeCl3溶液中通入足量C12后,充分加热除去过量的C12,不能得到纯净的FeC13溶液 | |
| D. | 饱和氯水既有酸性又有漂白性,加入适量NaHCO3固体,其漂白性增强 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 分散质粒子能做不停的,无规则的运动 | |
| B. | 是否有丁达尔现象 | |
| C. | 静置后既不分层,也无沉淀产生 | |
| D. | 分散质粒子直径在10-7-10-9m之间 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
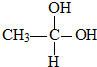 →CH3-CHO+H2O
→CH3-CHO+H2O
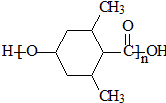 ]
]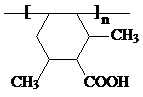 ;
;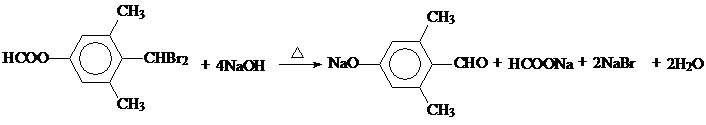 ;
; ;
;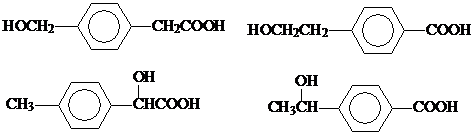 (任写一个).
(任写一个).查看答案和解析>>
科目:高中化学 来源: 题型:填空题
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
| 物质浓度(mol/L)时间(min) | NO | N2 | CO2 |
| 0 | 1.00 | 0 | 0 |
| 10 | 0.58 | 0.21 | 0.21 |
| 20 | 0.40 | 0.30 | 0.30 |
| 30 | 0.40 | 0.30 | 0.30 |
| 40 | 0.32 | 0.34 | 0.17 |
| 50 | 0.32 | 0.34 | 0.17 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 宇宙原子总数的88.6%是氢 | B. | 地球上的元素绝大多数是金属 | ||
| C. | 普鲁特“氢是元素之母”的预言 | D. | 宇宙中存在少量稀有气体分子 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com