
(1)反应原理:C2H5OH+NaBr+H2SO4![]() NaHSO4+C2H5Br+H2O
NaHSO4+C2H5Br+H2O
(2)主要装置见下图
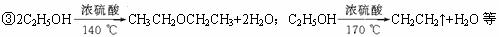
(3)操作步骤
①在100 mL圆底烧瓶中加入10 mL 95%乙醇、28 mL 78%硫酸,然后加入研细的13 g溴化钠。②加入几粒碎瓷片,小心摇动烧瓶使其均匀。将烧瓶与直形冷凝管相连,冷凝管下端连接接受器。③小心加热,使其充分反应,再进行蒸馏,直到无溴乙烷流出为止。④再将锥形瓶中液体冷却后倒入亚硫酸钠溶液中洗涤分液。
试回答下列问题:
①本实验用的是78%的硫酸,为何不用浓硫酸?________________________________。
②亚硫酸钠溶液的作用是____________________________________________________。
③该实验中会产生许多生成有机物的副反应,写出化学方程式:________________________________(举一例)。
④本次实验只收集到5 mL溴乙烷,比理想产量约10 mL少,原因是溴乙烷易挥发的缘故,为了减少其损失,你认为可采取什么措施?________________________________。
 名校课堂系列答案
名校课堂系列答案科目:高中化学 来源:物理教研室 题型:022
查看答案和解析>>
科目:高中化学 来源:物理教研室 题型:022
查看答案和解析>>
科目:高中化学 来源:101网校同步练习 高二化学 山东科学技术出版社 鲁教版 题型:058
溴乙烷是重要的化工原料,实验室制取溴乙烷(沸点为38.4℃)的原理及步骤如下:
(1)反应原理
C2H5OH+NaBr+H2SO4![]() NaHSO4+C2H5Br+H2O
NaHSO4+C2H5Br+H2O
(2)主要反应装置如图:
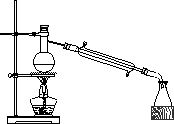
(3)操作步骤
①在100 mL的圆底烧瓶中加入10 mL 95%的乙醇.28 mL 78%的硫酸,然后加入研细的13 g溴化钠.
②加入几块碎瓷片,小心摇动烧瓶使其混合均匀.将烧瓶与直形冷凝管相连,冷凝管下端连接尾接管.
③小心加热,使其充分反应,再进行蒸馏,直到无溴乙烷流出为止.
④再将锥形瓶中的液体冷却后倒入亚硫酸钠溶液中洗涤分液.
试回答下列问题:
(1)本实验中用的是78%的硫酸,为何不用浓硫酸?________.
(2)亚硫酸钠溶液的作用是________.
(3)该实验中会发生许多生成有机物的副反应,写出有关化学方程式________(举两例)
(4)本实验只收集到5 mL溴乙烷,比理想产量约10 mL少,原因是溴乙烷易挥发,为了减少其损失,你认为可采取什么措施?________.
查看答案和解析>>
科目:高中化学 来源: 题型:
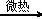 NaHSO4+C2H5Br+H2O
NaHSO4+C2H5Br+H2O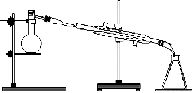
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com