
| 弱电解质 | CoC2O4 | Fe(OH)3 | NH3•H2O | H2C2O4 |
| 平衡常数 | Ksp=6.3×10-8 | Ksp=2.79×10-39 | Ka=1.7×10-5 | Ka1=5.6×10-2 Ka2=5.4×10-5 |
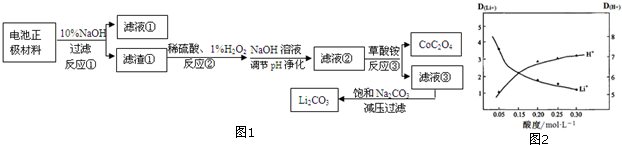
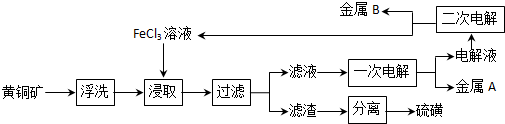
分析 根据题中流程可知,废旧锂电池正极材料(含LiCoO2、Al、Cu、Fe等)用氢氧化钠溶液浸泡,铝与氢氧化钠反应生成 偏铝酸钠,所以滤液①为Na[Al(OH)4]溶液,过滤得滤渣①为LiCoO2、Cu、Fe固体,滤渣中加酸溶解,再加双氧水氧化亚铁离子,同时还原Co3+,调节pH值,净化除去铜元素和铁元素得LiSO4、CoSO4溶液,再加入草酸铵得CoC2O4沉淀,过滤得滤液③为Li2SO4、(NH4)2C2O4、(NH4)2SO4溶液,在滤液中加入碳酸钠溶液,经减压过滤可得Li2CO3,据此答题;
解答 解:根据题中流程可知,废旧锂电池正极材料(含LiCoO2、Al、Cu、Fe等)用氢氧化钠溶液浸泡,铝与氢氧化钠反应生成 偏铝酸钠,所以滤液①为Na[Al(OH)4]溶液,过滤得滤渣①为LiCoO2、Cu、Fe固体,滤渣中加酸溶解,再加双氧水氧化亚铁离子,同时还原Co3+,调节pH值,净化除去铜元素和铁元素得LiSO4、CoSO4溶液,再加入草酸铵得CoC2O4沉淀,过滤得滤液③为Li2SO4、(NH4)2C2O4、(NH4)2SO4溶液,在滤液中加入碳酸钠溶液,经减压过滤可得Li2CO3,
(1)根据上面的分析可知,滤液①的主要成分是Na[Al(OH)4],滤液③为Li2SO4、(NH4)2C2O4、(NH4)2SO4溶液,所以滤液③中的阴离子除OH-外主要还含有C2O42-、SO42-,
故答案为:Na[Al(OH)4];C2O42-、SO42-;
(2)反应②中H2O2改用盐酸代替,会产生氯气污染空气,同时盐酸不能氧化亚铁离子,反应②中钴元素化合物与H2O2反应的化学方程式为2 LiCoO2+3H2SO4+H2O2=2 CoSO4+O2↑+Li2SO4+4H2O,
故答案为:盐酸反应后会产生有毒气体Cl2同时盐酸不能氧化二价亚铁;2 LiCoO2+3H2SO4+H2O2=2 CoSO4+O2↑+Li2SO4+4H2O;
(3)减压过滤就是抽滤,抽滤操作与普通过滤相比,除了得到沉淀较干燥外,还有一个优点是过滤速度快,
故答案为:过滤速度快;
(4)若滤液②中c(Co2+)=3.0mol•L-1,加入等体积的(NH4)2C2O4后,钴的沉降率达到99.9%,则沉淀后溶液中c(Co2+)=3.0×$\frac{1}{2}$×0.1%mol•L-1=1.5×10-3 mol•L-1,所以滤液③中 c(C2O42-)=$\frac{Ksp(CoC{\;}_{2}O{\;}_{4})}{c(C{o}^{2+})}$=4.2×10-5 mol•L-1,
故答案为:4.2×10-5 mol•L-1;
(5)萃取液酸度控制在0.05mol•L-1的可以抑制铁离子的水解,同时,根据图可知,此酸度时,Li+的萃取率较高,
故答案为:可抑制萃取剂中Fe3+水解,同时此酸度时,Li+的萃取率较高;
(6)由于氨水的Ka=1.7×10-5,草酸的Ka2=5.4×10-5,所以铵根离子的水解程度大于草酸根离子的水解程度,所以(NH4)2C2O4溶液pH<7,
故答案为:<.
点评 本题CoC2O4和Li2CO3的制备为载体,考查氧化还原反应、化学工艺流程、离子浓度计算、盐类的水解等,侧重考查学生对化学反应原理的理解,注意仔细审题,从题目中获取关键信息,难度中等.


 浙江名校名师金卷系列答案
浙江名校名师金卷系列答案 全优冲刺100分系列答案
全优冲刺100分系列答案科目:高中化学 来源: 题型:多选题
| A. | pH=5的NaHSO3溶液中:c(HSO3-)>c(SO32-)>c(H2SO3) | |
| B. | 同浓度的下列溶液中,①NH4HSO4 ②NH4Cl ③NH3•H2O c(NH4+)由大到小的顺序是:②>①>③ | |
| C. | 0.2 mol/L CH3COOH溶液和0.2 mol/L CH3COONa溶液等体积混合(忽略混合时体积变化):c(CH3COO-)+c(OH-)-c(H+)=0.1 mol•L-1 | |
| D. | pH相等的CH3COONa、NaOH和Na2CO3三种溶液:c(NaOH)<c(CH3COONa)<c(Na2CO3) |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 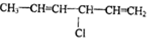 | B. | 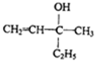 | ||
| C. | 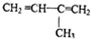 | D. | 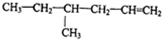 |
查看答案和解析>>
科目:高中化学 来源: 题型:实验题
 2-硝基甲苯和4-硝基甲苯均可用于印染行业,实验室利用下列反应和装置制备这两种物质
2-硝基甲苯和4-硝基甲苯均可用于印染行业,实验室利用下列反应和装置制备这两种物质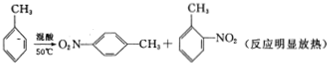
| 相对分子质量 | 密度/g•cm-3 | 沸点/℃ | 溶解性 | |
| 甲苯 | 92 | 0.866 | 110.6 | 不溶于水,易溶于硝基甲苯 |
| 2-硝基甲苯 | 137 | 1.162 | 222 | 不溶于水,易溶于液态烃 |
| 4-硝基甲苯 | 137 | 1.286 | 237.7 | 不溶于水,易溶于液态烃 |
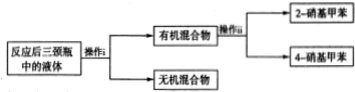
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
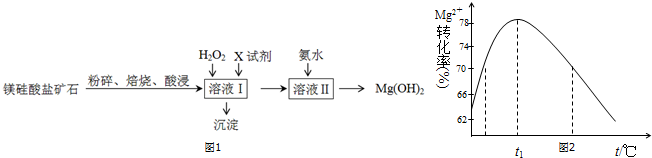
| Fe3+ | Al3+ | Fe2+ | Mg2+ | |
| 开始沉淀时 | 1.5 | 3.3 | 6.5 | 9.4 |
| 沉淀完全时 | 3.7 | 5.2 | 9.7 | 12.4 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 含有共价键的晶体,一定是原子晶体 | |
| B. | 离子晶体中,一定存在金属元素和非金属元素 | |
| C. | 同时含有离子键和共价键的化合物,既可能是离子化合物,也可能是共价化合物 | |
| D. | 在共价化合物中一定存在共价键,但含有共价键的不一定是共价化合物 |
查看答案和解析>>
科目:高中化学 来源: 题型:多选题
| A. | 研制乙醇汽油技术,能够降低机动车尾气中有害气体的排放 | |
| B. | 联合制碱法生产纯碱时,在饱和食盐水中先通入二氧化碳,再通入氨气 | |
| C. | 接触法制备硫酸的过程中,在吸收塔内是用大量的水吸收三氧化硫 | |
| D. | 工业上通过电解熔融氧化铝制备金属铝时,常常加入冰晶石作助熔剂 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 氟氯烃的肆意排放会加速臭氧层的破坏,使大气层中的紫外线增强 | |
| B. | 不慎将苯酚沾到皮肤上应立即用酒精清洗 | |
| C. | 淀粉、蛋白质、油脂均是天然高分子化合物 | |
| D. | 除去乙酸乙酯中少量的乙酸:用饱和碳酸钠溶液洗涤后分液、干燥、蒸馏即可 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com