
以下表格中的实验是以CuSO4为例,分析电解质在溶液里所起反应的实质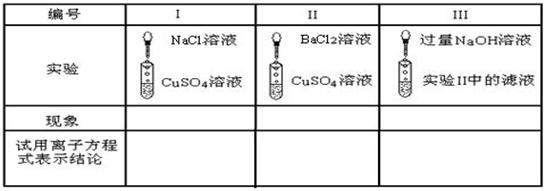
无明显现象;产生白色沉淀;产生蓝色沉淀。无;Ba2++SO42—=BaSO4↓;Cu2++2OH—=Cu(OH)2↓
【解析】
试题分析:氯化钠和硫酸铜溶液不反应,则无现象;氯化钡和硫酸铜反应生成白色沉淀硫酸钡,反应的离子方程式是Ba2++SO42—=BaSO4↓;Ⅱ的滤液中含有氯化铜,所以加入氢氧化钠溶液,则生成蓝色沉淀氢氧化铜,反应的离子方程式是Cu2++2OH—=Cu(OH)2↓。
考点:考查离子反应的有关判断和离子方程式的书写
点评:该题是基础性试题的考查,难度不大。试题注重教材基础知识的巩固和训练,侧重能力的培养,有助于培养学生的规范答题能力,也有利于提高学生的应试能力。


 成功训练计划系列答案
成功训练计划系列答案 倍速训练法直通中考考点系列答案
倍速训练法直通中考考点系列答案 一卷搞定系列答案
一卷搞定系列答案 名校作业本系列答案
名校作业本系列答案 轻巧夺冠周测月考直通名校系列答案
轻巧夺冠周测月考直通名校系列答案科目:高中化学 来源: 题型:
| 编号 | Ⅰ | Ⅱ | Ⅲ |
| 实验 |  NaCl溶液 NaCl溶液CuSO4溶液 |
 BaCl2溶液 BaCl2溶液CuSO4溶液 |
 过量NaOH 溶液 过量NaOH 溶液实验Ⅱ中的溶液 |
| 现象 | |||
| 试用离子方程式表示结论 |
查看答案和解析>>
科目:高中化学 来源:2012-2013学年甘肃省兰州五十五中高一上学期期末考试化学试卷(带解析) 题型:填空题
以下表格中的实验是以CuSO4为例,分析电解质在溶液里所起反应的实质
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com