
| A�� | �ɷ���ʽ�ٿ�֪��H2O2�������Ա�Fe3+ǿ | |
| B�� | ��H2O2�ֽ�����У���Һ��H+�����ʵ��������� | |
| C�� | ��H2O2�ֽ�����У�Fe2+��Fe3+���������ֲ��� | |
| D�� | H2O2��������Ҫ�ϸ�������Fe2+ |
���� A�����ݷ�Ӧ�������������Ա���������ǿ�жϣ�
B������2Fe2++H2O2+2H+��2Fe3++2H2O��2Fe3++H2O2��2Fe2++O2��+2H+�ڣ����ܷ�ӦΪ2H2O2�T2H2O+O2�����ݴ��жϣ�
C���ܷ�ӦΪ2H2O2�T2H2O+O2����Fe2+ΪH2O2�ֽ�Ĵ�����Fe2+��Fe3+���������ֲ��䣻
D��Fe2+ΪH2O2�ֽ�Ĵ�����
��� �⣺A����Ӧ2Fe2++H2O2+2H+�T2Fe3++2H2O�У�Fe2+��H2O2��������Fe3+����H2O2�������Ա�Fe3+ǿ����A����
B��2Fe2++H2O2+2H+��2Fe3++2H2O��2Fe3++H2O2��2Fe2++O2��+2H+�ڣ��ܷ�ӦΪ2H2O2�T2H2O+O2������Һ��H+Ũ�Ȼ������䣬��B����
C���ܷ�ӦΪ2H2O2�T2H2O+O2����Fe2+ΪH2O2�ֽ�Ĵ�����Fe2+��Fe3+���������ֲ��䣬��C��ȷ��
D��Fe2+ΪH2O2�ֽ�Ĵ������ɵ���H2O2�ֽ⣬����H2O2��������Ҫ�ϸ�������Fe2+����D��ȷ��
��ѡB��
���� ���⿼��������ԭ��Ӧ�Լ���ѧ��Ӧ��̽������Ŀ�Ѷ��еȣ�ע��ӻ��ϼ۵ĽǶȷ���������ԭ��Ӧ��



| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ���ѡ��
| A�� | ����pH=1��CH3COOH��Һ��pH=13��NaOH��Һ���������Ƶ� | |
| B�� | c��OH-����c��H+�� | |
| C�� | c��Na+����c��CH3COO-�� | |
| D�� | c��H+��+c��CH3COO-��=c��OH-�� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | F-��I-��S2- | B�� | Fe3+��MnO4-��HNO2 | C�� | ClO-��Mg��H2O2 | D�� | Cl2��Fe2+��Al |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | K+��SO42-��Fe3+��Na+ | B�� | Ca2+��NO3-��AlO2-��Cl- | ||
| C�� | NO3-��I-��K+��Mg2+ | D�� | K+��SO42-��Na+��Cl- |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| ѡ�� | ���� | Ҫ�� |
| A | K+��Cl-��SO42-��MnO4- | c��K+����c��Cl-�� |
| B | Na+��Ca2+��I-��NO3- | c��H+��/c��OH-��=1��1014 |
| C | Al3+��NH4+��SO42-��CH3COO- | �μ�NaOHŨ��Һ������������� |
| D | Na+��HCO3-��Cl-��SO42- | �μ�Al2��SO4��3��Һ�����г������������ |
| A�� | A | B�� | B | C�� | C | D�� | D |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | 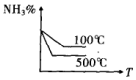 | B�� | 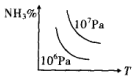 | C�� | 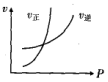 | D�� | 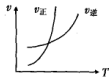 |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | ��ˮ���Ȼ�淋Ļ����Һ��������c��Cl-����c��NH4+�� | |
| B�� | 0.2 mol/L��������������Һ�У�c��OH -��+c��SO32-��=c��H+��+c��H2SO3�� | |
| C�� | ��0.2 mol/LNaHCO3��Һ�м�������0.1 mol/LNaOH��Һ��c��CO32-����c��HCO3-����c��OH-����c��H+�� | |
| D�� | �����£�0.05 mol/LCH3COONa��0.05 mol/LCH3COOH����������Һ��c�� CH3COO-��+c��CH3COOH��=0.1 mol/L |
�鿴�𰸺ͽ���>>
����ѧУ��ѡ - ��ϰ���б� - �����б�
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com