
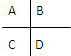
 右边是周期表中的短周期的一部分,若这些元素的原子之间均能形成共价键,则形成的共用电子对偏移程度最大的是( )
右边是周期表中的短周期的一部分,若这些元素的原子之间均能形成共价键,则形成的共用电子对偏移程度最大的是( )| A、BC | B、BD | C、AD | D、AB |
 孟建平名校考卷系列答案
孟建平名校考卷系列答案科目:高中化学 来源: 题型:
| 3 |
| 4 |


| ||
| ||
查看答案和解析>>
科目:高中化学 来源:高中化学必修2期中模拟 题型:013
|
镭是周期表中第七周期的ⅡA族元素,下列关于镭的性质的描述中不正确的是 | |
| [ ] | |
A. |
在化合物中呈+2价 |
B. |
单质与水反应放出氢气 |
C. |
氢氧化物呈两性 |
D. |
碳酸盐难溶于水 |
查看答案和解析>>
科目:高中化学 来源:2012-2013学年江西省南昌市第二中学高一下学期期中考试化学试卷(带解析) 题型:单选题
右边是周期表中的短周期的一部分,若这些元素的原子之间均能形成共价键,则形成的共用电子对偏移程度最小的是: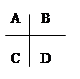
| A.BC | B.BD | C.AD | D.AB |
查看答案和解析>>
科目:高中化学 来源:2015届江西省南昌市高一下学期期中考试化学试卷(解析版) 题型:选择题
右边是周期表中的短周期的一部分,若这些元素的原子之间均能形成共价键,则形成的共用电子对偏移程度最小的是:
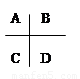
A.BC B.BD C.AD D.AB
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com