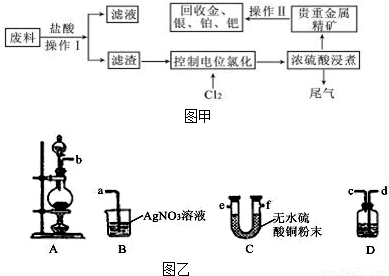
解:(1)由工业流程可知,在浓硫酸浸煮产生二氧化硫尾气,利用NaOH溶液来吸收二氧化硫,完成尾气处理,故答案为:c;e;
(2)实验操作I物过滤,过滤操作需要漏斗、玻璃棒、烧杯等仪器,故答案为:过滤;漏斗、玻璃棒、烧杯;
(3)实验室利用二氧化锰与浓盐酸制取氯气,该离子反应为MnO
2+4H
++2Cl
-
Mn
2++Cl
2↑+2H
2O,故答案为:MnO
2+4H
++2Cl
-
Mn
2++Cl
2↑+2H
2O;
①因为要检验混合中的水和HCl,应先检验水(利用无色硫酸铜),然后通过装置D除去氯气(可选有机试剂),最后用硝酸银溶液检验HCl的存在,所以顺序为b接e,f接d,c接a(或b接f,e接d,c接a),故答案为:e;f;d;c;
②装置D为吸收氯气,避免对HCl检验的干扰,故答案为:吸收氯气;
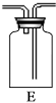
③在BD之间添加装置E,广口瓶中放入湿润的KI淀粉试纸(或湿润的有色布条),验证氯气已被除尽,不干扰HCl的检验,故答案为:BD;湿润的KI淀粉试纸(或湿润的有色布条).
分析:(1)由工业流程可知,在浓硫酸浸煮产生二氧化硫尾气,利用碱来吸收处理;
(2)实验操作I物过滤,使用漏斗、玻璃棒、烧杯完成操作;
(3)实验室利用二氧化锰与浓盐酸制取氯气;
①因为要检验混合中的水和HCl,应先检验水(利用无色硫酸铜),然后通过装置D除去氯气(可选有机试剂),最后用硝酸银溶液检验HCl的存在;
②装置D为吸收氯气;
③在BD之间添加装置E,验证氯气已被除尽.
点评:本题以实际生产为背景考查物质的制备、实验仪器的连接等,注意物质性质与装置的选择、检验物质时排除其它物质的干扰,题目难度较大.

 Mn2++Cl2↑+2H2O,故答案为:MnO2+4H++2Cl-
Mn2++Cl2↑+2H2O,故答案为:MnO2+4H++2Cl- Mn2++Cl2↑+2H2O;
Mn2++Cl2↑+2H2O;