
(15分)硫代硫酸钠是一种重要的化工产品。工业上常利用含硫废水生产Na2S2O3?5H2O,实验室可用如下装置(略去部分加持仪器)模拟生成过程。

烧瓶C中发生反应如下:
Na2S(aq)+H2O(l)+SO2(g)=Na2SO3(aq)+H2S(aq) (I)
2H2S(aq)+SO2(g)=3S(s)+2H2O(l) (II)
S(s)+Na2SO3(aq) Na2S2O3(aq) (III)
Na2S2O3(aq) (III)
(1)仪器组装完成后,关闭两端活塞,向装置B中的长颈漏斗内注入液体至形成 一段液注,若 ,则整个装置气密性良好。装置D的作用是 。装置E中为 溶液。
(2)为提高产品纯度,应使烧瓶C中Na2S和Na2SO3恰好完全反应,则烧瓶C中Na2S和Na2SO3物质的量之比为 。
(3)装置B的作用之一是观察SO2的生成速率,其中的液体最好选择 。
a.蒸馏水 b.饱和Na2SO3溶液
c.饱和NaHSO3溶液 d.饱和NaHCO3溶液
(4)实验中,为使SO2缓慢进入烧瓶C,采用的操作是 。
(5)已知反应(III)相对较慢,则烧瓶C中反应达到终点的现象是 。
(6)反应终止后,烧瓶C中的溶液经蒸发浓缩冷却,过滤,洗涤,干燥,即得到粗产品(主要含有Na2S2O3?5H2O和其他杂质)。某兴趣小组为测定该产品纯度,准确称取4.96 g产品,用适量蒸馏水溶解,以淀粉作指示剂,用0.1000 mol?L?1碘的标准溶液滴定。反应原理为:2S2O32-+I2=S4O62-+2I?,滴定至终点时,滴定起始和终点的液面位置如下图,则产品的纯度为_________。

经仪器分析,该产品纯度为16%,分析该兴趣小组测定产品纯度偏差的原因(忽略人为误差) 。[M(Na2S2O3?5H2O)=248g/mol]
(1)液柱高度保持不变(1分) 防止倒吸(1分) NaOH(合理即得分)(1分)(2)2:1(2分)
c(2分)(4)控制滴加硫酸的速度(合理即得分)(2分) 溶液变澄清(或浑浊消失)(2分)
(6)18.1% (2分) 粗产品中含有Na2SO3(或Na2S)可以消耗I2,使消耗的碘水体积偏大(2分)
【解析】
试题分析:(1)如果装置不漏气,则液注高度保持不变,据此可以说明气密性良好;SO2易溶于水,所以D为安全瓶,起防止倒吸的作用;SO2、H2S均是大气污染物,需要尾气处理,因此装置E起到吸收尾气中SO2、H2S的作用。二者都是酸性气体,应该选用NaOH溶液。
(2)根据题目所给3个化学反应方程式可得出对应关系:2Na2S ~ 2H2S ~ 3S ~3 Na2SO3,即2molNa2S反应时同时生成2molNa2SO3,还需要1molNa2SO3,所以烧瓶C中Na2S和Na2SO3物质的量之比为2:1。
(3)SO2易溶于水,能与Na2SO3溶液、NaHCO3溶液反应,但在NaHSO3溶液中溶解度较小,所以最好选用饱和亚硫酸氢钠溶液,答案选c;
(4)SO2利用70% H2SO4与Na2SO3反应制取,所以为使SO2缓慢进入烧瓶C,采用的操作是控制滴加硫酸的速度即可;
(5)反应(III)相对较慢,而反应III 是固体S与亚硫酸钠溶液反应,所以烧瓶C中反应达到终点的现象是溶液变澄清(或浑浊消失);
(6)根据示意图可知起始时读数是0.00ml,终点时读数是18.10ml,这说明实际消耗溶液的体积是18.10ml,所以Na2S2O3?5H2O的质量=0.1000mol/L×0.01810L×2×248g/mol=0.89776g,则产品的纯度为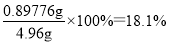 。如果经仪器分析,该产品纯度为16%,这说明测量值偏高,即消耗标准液的体积偏大,所以可能的原因是粗产品中含有Na2SO3(或Na2S)可以消耗I2,使消耗的碘水体积偏大。
。如果经仪器分析,该产品纯度为16%,这说明测量值偏高,即消耗标准液的体积偏大,所以可能的原因是粗产品中含有Na2SO3(或Na2S)可以消耗I2,使消耗的碘水体积偏大。
考点:考查物质制备实验方案设计与探究


科目:高中化学 来源:2014-2015广东省增城市高一上学期期末化学试卷(解析版) 题型:选择题
下列实验目的无法实现的是
A.用激光笔光束鉴别氯化铁溶液和氢氧化铁胶体
B.用KSCN溶液鉴别Fe3+和Fe2+
C.用氨水鉴别Al3+和Mg2+
D.用焰色反应鉴别碳酸钠溶液和碳酸钾溶液
查看答案和解析>>
科目:高中化学 来源:2014-2015甘肃省高一上学期期末考试化学试卷(解析版) 题型:选择题
下列不涉及氧化还原反应的是
A.自然界中“氮的固定” B.用铂丝蘸取NaCl溶液进行焰色反应
C.食物腐败变质 D.铜铸塑像上出现铜绿[Cu2(OH)2CO3]
查看答案和解析>>
科目:高中化学 来源:2014-2015福建省高二上学期期中化学(理)试卷(解析版) 题型:选择题
已知反应A+3B 2C+D,在某段时间内以A的浓度变化表示的化学反应速率为1mol·L-1·min-1,则此段时间内以C的浓度变化表示的化学反应速率为
2C+D,在某段时间内以A的浓度变化表示的化学反应速率为1mol·L-1·min-1,则此段时间内以C的浓度变化表示的化学反应速率为
A.0.5mol·L-1·min-1 B.1mol·L-1·min-1
C.2mol·L-1·min-1 D.3mol·L-1·min-1
查看答案和解析>>
科目:高中化学 来源:2014-2015福建省高二上学期期中化学(理)试卷(解析版) 题型:选择题
下列说法正确的是
A、热化学方程式的计量数可以表示分子的个数
B、热化学方程式中只需标明生成物的状态
C、反应热指的是反应过程中放出或吸收的热量
D、伴随能量变化的一定是化学变化
查看答案和解析>>
科目:高中化学 来源:2014-2015学年湖北省高三元月调考理综化学试卷(解析版) 题型:选择题
下列实验中,依据实验操作及现象,得出的结论正确的是
操作 | 现象 | 结论 | |
A | 将水蒸气通过灼热的铁粉 | 粉末变红 | 铁与水在高温下发生反应 |
B | 将充满NO2的密闭玻璃球浸泡在热水中 | 红棕色变深 | 反应2NO2(g) |
C | 将少量的溴水分别滴入FeCl2溶液、NaI溶液中,再分别滴加CCl4振荡 | 上层分别呈无色和紫红色 | 还原性:I->Br- >Fe2+ |
D | 向溶液X中加入稀盐酸,并将产生的无色气体通入澄清石灰水中 | 生成白色沉淀 | 溶液X中一定含有 CO32-或 SO32- |
查看答案和解析>>
科目:高中化学 来源:2014-2015学年河南省郑州市高三第一次质量预测化学试卷(解析版) 题型:填空题
(9分)已知某溶液中可能含有NO3- 、Cl- 、SO42-、CO32-、NH4+、Fe3+、Al3+和K+中的几种,且所含阴离子的物质的量相等。为确定该溶液的成分,某学习小组做了如下实验:
①取该溶液100 mL,加入过量NaOH溶液,加热,得到0.02mol气体,同时产生红褐色沉淀;
②将沉淀过滤、洗涤、灼烧,得到1.6 g固体;
③向上述滤液中加入足量BaCl2溶液,得到4.66 g不溶于盐酸的沉淀。
请回答下列问题:
(1)结合①和②,判断原溶液中肯定含有的离子是 ,可以排除的离子是 。
(2)由③推知原溶液中一定有 离子,其物质的量为 mol。
(3)综合(1)、(2)及题干信息,结合溶液中电荷守恒知识,还可以排除的离子是 。该学习小组最终得出结论:该溶液由 种阳离子(填数字,下同)和 种阴离子组成。
查看答案和解析>>
科目:高中化学 来源:2014-2015学年河南省郑州市高三第一次质量预测化学试卷(解析版) 题型:选择题
化学与生产、生活密切相关。对下列现象或事实解释不正确的是
选项 | 现象或事实 | 解释 |
A | 用活性炭去除冰箱中的异味 | 活性炭具有吸附性 |
B | 漂白粉在空气中久置变质 | 漂白粉中的Ca(ClO)2 与空气中的 CO2及H2O反应生成CaCO3和HClO,HClO易分解 |
C | FeCl3溶液可用于制作铜质印刷线路板 | FeCl3溶液能将铜氧化为Cu2+ |
D | 用热碱水清除炊具上残留的油污 | Na2CO3可和油污直接发生反应 |
查看答案和解析>>
科目:高中化学 来源:2014-2015学年福建省福州市高三上学期期末考试化学试卷(解析版) 题型:填空题
(8分)84消毒液是一种以次氯酸钠为主要成分的高效消毒剂。
(1)次氯酸钠溶液呈碱性,原因可用离子方程式表示为 ;
(2)二氧化碳、氢氧化钠、氯化钠三种物质中,添加到84消毒液中可增强其消毒效果的是 ;
(3)84消毒液可以通过电解氯化钠稀溶液制取,电解装置通常选用铁和碳棒为电极,电解时铁电极反应式为 。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com