
【题目】工业合成氨的反应为:N2+3H2![]() 2NH3,该反应在一定条件下的密闭容器中进行。下列关于该反应的说法正确的是( )
2NH3,该反应在一定条件下的密闭容器中进行。下列关于该反应的说法正确的是( )
A. 达到平衡时,反应速率:v(正)=v(逆)=0
B. 使用催化剂可加快反应速率,提高生产效率
C. 为了提高H2的转化率,应适当增大H2的浓度
D. 若在密闭容器加入1molN2和过量的H2,最后能生成2molNH3
科目:高中化学 来源: 题型:
【题目】一种熔融碳酸盐燃料电池原理示意如图.下列有关该电池的说法正确的是( )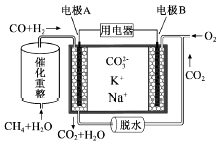
A.电极B上发生的电极反应为:O2+2CO2+4e﹣=2CO32﹣
B.电极A上H2参与的电极反应为:H2+2OH﹣﹣2e﹣=2H2O
C.电池工作时,CO32﹣向电极B移动
D.反应CH4+H2O ![]() 3H2+CO,每消耗1molCH4转移12mol 电子
3H2+CO,每消耗1molCH4转移12mol 电子
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】X、Y、Z、D、E、F是原子序数依次增大的六种常见元素。E的单质在Z2中燃烧的产物可使品红溶液褪色。F和Z元素形成的化合物F3Z4具有磁性。X的单质在Z2中燃烧可生成XZ和XZ2两种气体。D的单质是一种金属,该金属在XZ2中剧烈燃烧生成黑、白两种固体。请回答下列问题:
(1)F元素在周期表中的位置是________,Y的单质分子的结构式为__________,DZ的电子式为________,DZ化合物中离子半径较大的是________(填离子符号)。
(2)X元素形成的同素异形体的晶体类型可能是________(填序号)。
①原子晶体 ②离子晶体 ③金属晶体 ④分子晶体
(3)X、Y、Z形成的10电子氢化物中,X、Y的氢化物沸点较低的是(写化学式):__________;Y、Z的氢化物分子结合H+能力较强的是(写化学式)________。
(4)下列可作为比较D和Na金属性强弱的依据是________。(填序号)
a.测两种元素单质的硬度和熔、沸点
b.比较两元素最高价氧化物对应的水化物溶液的碱性强弱
c.比较两种元素在氯化物中化合价的高低
d.比较单质与同浓度盐酸反应的剧烈程度
(5)Y的氢化物和Z的单质在一定条件下反应生成Z的氢化物(产物之一),该反应的方程式为___________。
(6)有人建议将氢元素排在元素周期表的ⅣA族,请你从化合价的角度给出一个理由__________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】反应H2(g)+I2(g)![]() 2HI(g)在温度和容积不变的条件下进行。能说明反应达到平衡状态的叙述是( )
2HI(g)在温度和容积不变的条件下进行。能说明反应达到平衡状态的叙述是( )
A. c(H2)=c(I2) B. H2的消耗速率等于HI的分解速率
C. 容器内气体的颜色不再变化 D. 容器内压强不再变化
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】贵州的矿产资源丰富,在全国占优势地位的有铝、磷、煤、锰、重晶石、黄金、铅锌、锑等众多品种。回答下列问题:
(1)金元素属于铜族元素,原子结构与铜相似,在元素周期表中位于第六周期,基态金原子的外围电子排布图为__________;Cu2+能与多种离子或分子形成稳定性不同的配合物。经X射线衍射测得配合物酞菁铜的晶体结构,其局部结构如图所示:
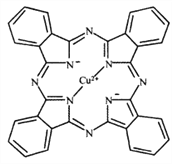
①酞菁铜结构中非金属元素电负性由大到小的顺序为__________;
②酞菁铜结构中N原子的轨道杂化类型为__________。酞菁铜结构中不存在的化学键类型为__________
A.配位键 B.金属键 C.σ键 D.π键
(2)煤通过干馏、气化、液化可获得清洁燃料和多种化工原料,氨是其中之一。NH3的 VSEPR模型为__________。
(3)锰、铁两元素中第三电离能较大的是__________(填元素符号),原因是___________。
(4)碲化锌(ZnTe)具有宽禁带的特性,常用于制作半导体材料,碲化锌晶体有立方和六方两种晶型,其立方晶胞结构如下图所示。
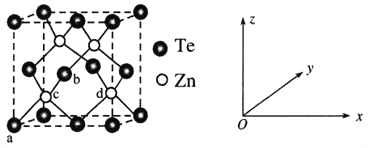
①原子坐标参数表示晶胞内部各原子的相对位置。已知a、b、c的原子坐标参数分别为(0,0,0)、(![]() ,0,
,0,![]() )、(
)、(![]() ,
,![]() ,
,![]() )。则d的原子坐标参数为__________。
)。则d的原子坐标参数为__________。
②若两个距离最近的Te原子间距离为apm,则晶体密度为__________g/cm3(列式即可)。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某原电池装置如图所示,电池总反应为2Ag+Cl2===2AgCl。下列说法正确的是
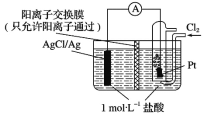
A. 正极反应为AgCl+e-===Ag+Cl-
B. 负极反应为Ag-e-===Ag+
C. 放电时,交换膜右侧溶液中有大量白色沉淀生成
D. 当电路中转移0.01 mol e-时,交换膜左侧溶液中约减少0.02 mol离子
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com