
【题目】(工业上常用铁质容器盛装冷浓硫酸。为研究铁质材料与热浓硫酸的反应,某学习小组进行了以下探究活动:(1)将已去除表面氧化物的铁钉(碳素钢)放入冷浓硫酸中,10分钟后移入硫酸铜溶液中,片刻后取出观察,铁钉表面无明显变化,其原因是____________________。
(2)另称取铁钉6.0g放入15.0ml浓硫酸中,加热,充分应后得到溶液X并收集到气体Y。
①甲同学认为X中除Fe3+外还可能含有Fe2+,若要确认其中的Fe2+,应选用 (选填序号)。
a.KSCN溶水 b.KSCN溶液和铁粉
c.浓氨水 d.酸性KMnO4溶液
②乙同学取336ml(标准状况)气体Y通入足量溴水中,发生反应: SO2+Br2+2H2O=2HBr+H2SO4, 然后加入足量BaCl2溶液,经适当操作后得干燥固体2.33g。由此推知气体Y中SO2的体积分数为 。
分析上述实验中SO2体积分数的结果,丙同学认为气体Y中还可能含有H2和Q气体。为此设计了下列探究实验装置(图中夹持仪器省略)。

(3)装置B中试剂的作用是 。
(4)认为气体Y中还含有Q的理由是 (用化学方程式表示)。
(5)为确认Q的存在,需在装置中添加M于 (选填序号)。
a.A之前 b.A-B间 c.B-C间 d.C-D间
(6)如果气体Y中含有H2,预计实验现象应是 。
【答案】(1)铁钉表面形成致密的氧化物薄膜,阻止铁和硫酸铜反应
(2)①d ②66.7%(或2/3)(3)检验SO2是否除尽
(4)C+2H2SO4(浓)![]() CO2+2SO2+2H2O(5)c
CO2+2SO2+2H2O(5)c
(6)D中固体由黑变红和E中固体由白变蓝
【解析】
试题分析:(1)将已去除表面氧化物的铁钉(碳素钢)放入冷浓硫酸中,金属铁发生钝化你,表面形成致密的氧化膜,10分钟后移入硫酸铜溶液中,片刻后取出观察,铁钉表面无明显变化,铁被氧化膜包围,阻止金属铁与铜离子发生置换反应。(20)另称取铁钉6.0g放入15.0ml浓硫酸中,加热,氧化膜被破坏,铁和浓硫酸充分应后得到溶液可能为FeSO4 或 Fe2(SO4)3 或FeSO4 和 Fe2(SO4)3混合液,并收集到H2气体SO2 气体,随着反应进行,浓硫酸变为稀硫酸与铁继续反应生成 H2。,气体Y可能为SO2和H2的混合气体;
①Fe3+检验可以用KSCN溶液,Fe2+具有还原性,可以用酸性KMnO4溶液,氨水和Fe3+ 和Fe2+都能发生反应,生成沉淀,无法判断Fe2+的存在
②SO2+Br2+2H2O=2HBr+H2SO4, 然后加入足量BaCl2溶液,经适当操作后得干燥固体2.33g硫酸钡,折算为 0.01 mol,n(SO2)=0.01mol,,混合气体为0.015 mol,由此推知气体Y中SO2的体积分数为0.01/0.015=2/3;
(3)酸性高锰酸钾溶液能够吸收SO2,吸收是否完全,用品红检验;氢气能够还原氧化铜,黑色粉末变为红色,无水硫酸铜变为蓝色晶体,证明有氢气存在;铁中混有碳单质,在加热情况下,碳与浓硫酸反应生成二氧化碳,生成的气体中可能含有SO2 、H2 、CO2等气体的混合气体。为确认CO2的存在,需在装置中添加M于B-C间,SO2已经除尽,能够使石灰水变浑浊的气体只能为CO2


科目:高中化学 来源: 题型:
【题目】液体燃料电池相比于气体燃料电池具有体积小等优点。一种以液态肼(N2H4)为燃料的电池装置如图所示。下列有关叙述正确的是( )
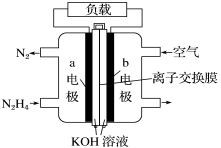
A.该燃料电池放电时,正极发生氧化反应,pH变大
B.a极的反应式:N2H4+4OH--4e-=N2↑+4H2O
C.放电时,电流从a极经过负载流向b极
D.其中的离子交换膜需选用阳离子交换膜
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】将4 molA气体和2 molB气体在2L的容器中混合并在一定条件下发生如下反应:2A(g)+B(g) ![]() 2C(g),若经2s(秒)后测得C的浓度为0.6 mol.L-1现有下列几种说法:
2C(g),若经2s(秒)后测得C的浓度为0.6 mol.L-1现有下列几种说法:
①用物质A表示的反应的平均速率为0.3mol.L-1.S-1
②用物质B表示的反应的平均速率为0.6mol.L-1.S-1
③2s时物质A的转化率为70%
④2s时物质B的浓度为0.7mol.L-1
其中正确的是 ( )
A.①③ B.①④ C、②③ D.③④
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列实验中,可以加快反应速率的是( )
A.钠与水反应时,增加水的量
B.锌与稀硫酸反应时,加入少量CuSO4固体
C.用18mol/L的硫酸溶液代替2mol/L硫酸溶液常温下与铝反应
D.锌与稀硫酸反应时,加入少量醋酸钠固体
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】发展“绿色食品”是提高人类生存质量的重要措施,绿色食品指( )
A.绿颜色的营养食品 B.含叶绿素的营养食品
C.植物类营养食品 D.安全无公害的营养食品
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】我国积极启动“蓝天工程”和“绿水工程”,是为了保护生态环境、提高全体人民生活质量的重要举措。下列措施不利于以上工程实施的是
A.推广使用燃煤脱硫技术,防治SO2污染
B.减少重金属、农药和难分解有机物的排放
C.加大石油、煤炭的开采速度,增加化石燃料的供应量
D.开发新能源和新致冷剂,减少CO2和氟氯烃等物质的大量排放
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】工业上一般在恒容密闭容器中可以采用下列反应合成甲醇:CO(g)+2H2(g) ![]() CH3OH(g) ΔH
CH3OH(g) ΔH
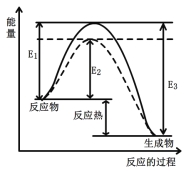

图1 (图中表示生成1mol物质时的能量) 图2
(1)根据图1请写出合成甲醇的热化学方程式 (热量用E1、E2或E3表示)。
(2)该反应的逆反应速率随时间变化的关系如上图2。t1时改变了某种条件,改变的条件可能是 。
(3)判断反应达到平衡状态的依据是 (填字母序号)。
A.2v(H2)(逆) =v(CO)(正)
B.混合气体的密度不变
C.混合气体的平均相对分子质量不变
D.CH3OH、CO、H2的浓度都不再发生变化
E.容器内CO、H2、CH3OH的浓度之比为1:2:1
(4)在一定温度下,若将4a mol H2和2amol CO放入2L的密闭容器中,充分反应后测得CO的转化率为50%,则该反应的平衡常数为 。若此时再向该容器中投入a mol CO、2amol H2和amol CH3OH,判断平衡移动的方向是 _______(“正向移动”“逆向移动”或“不移动”);与原平衡相比,CO的物质的量浓度 _____(填“增大”、“不变”或“减小”)。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在下列反应中,HCl作还原剂的是( )
A. NaOH + HCl = NaCl + H2O
B. Zn + 2HCl = ZnCl2 + H2↑
C. MnO2 + 4HCl(浓)![]() MnCl2 + 2H2O + Cl2↑
MnCl2 + 2H2O + Cl2↑
D. CuO + 2HCl = CuCl2 + H2O
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com