
【题目】在可逆反应中,改变下列条件一定能加快反应速率的是( )
A. 增大反应物的量 B. 升高温度 C. 增大压强 D. 使用催化剂
科目:高中化学 来源: 题型:
【题目】钢铁发生吸氧腐蚀时,正极上发生的电极反应是
A.4OH--4e-=2H2O+O2↑B.Fe2++2e-=Fe
C.2H2O+O2+4e-=4OH-D.Fe-2e-=Fe2+
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】Li3N是一种储氢材料,可以用Li和N2在450℃反应制备。已知Li3N易水解,细粉状的Li3N在空气中加热可发生剧烈燃烧。下图是某实验小组设计的实验室制备少量Li3N的装置图。请回答下列问题:
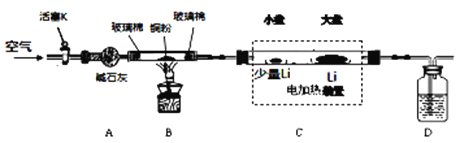
(1)B装置的作用是_________________,如果B装置中玻璃管两端没有玻璃棉可能造成的后果是____________________________。
(2)D装置中的试剂是_____________,作用是__________________________。
(3)C装置的小盘中放有少量Li的作用是____________________________。
(4)实验步骤如下:安装好仪器,检查装置气密性,装入药品;_________________________。(请按正确的顺序填入下列步骤的标号);拆除装置,取出产物。
①点燃B中酒精灯加热B中试管;
②打开活塞K;
③关闭电加热装置停,充分冷却;
④调节电加热装置控制温度为450℃;
⑤关闭活塞K;
⑥熄灭B中酒精灯;
(5)请你设计一个实验,用化学方法区分Li与Li3N,写出实验简要步骤及观察到的现象___________________________________。
(6)Li3N在H2中加热时可得到氨基锂(LiNH2),该反应在270℃可逆,所以Li3N可作为储氢材料,该反应的化学方程式为:___________________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】工业上电解制烧碱的技术是用离子交换膜法,主要原料是饱和食盐水.图为离子交换膜法电解原理示意图:
请回答下列问题: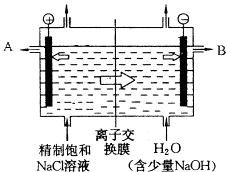
(1)电解槽中部的阳离子交换膜把电解槽隔成了阴极室和阳极室,这种阳离子交换膜,只允许溶液中的通过(填写下列微粒的编号).
①H2 , ②Cl2 , ③Cl﹣ , ④H+ , ⑤Na+ , ⑥OH﹣ .
(2)B极为电解槽的极,电极反应式为 .
(3)若用碱性氢氧燃料电池给予上述电解槽供电,燃料电池的正极反应式为:; 如果每小时能产生标准状况下的氯气V L,则每小时至少向燃料电池中输入氧气的物质的量(理论计算)mol.
(4)若将标准状况下13.44L的阳极气体通入热的氢氧化钠溶液中,反应中只有一种元素的化合价发生改变,得到了两种含氯化合物,其中还原产物与氧化产物物质的量之比为5:1,写出该反应的离子方程式
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】近年来高铁酸钾(K2FeO4)已经被广泛应用在水处理方面。高铁酸钾的氧化性超过高锰酸钾,是一种集氧化、吸附、凝聚、杀菌于一体的新型高效多功能水处理剂。干燥的高铁酸钾受热易分解,在198℃以下是稳定的。高铁酸钾在水处理过程中涉及的变化过程有( )
①蛋白质的变性 ②蛋白质的盐析 ③胶体聚沉 ④盐类水解 ⑤焰色反应 ⑥氧化还原反应
A.①②③④B.①③④⑥C.②③④⑤D.②③⑤⑥
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列实验操作规范且能达到目的的是( )
目的 | 操作 | |
A. | 取20.0 mL盐酸 | 用50ml量筒量取,读数时仰视刻度线 |
B. | 清洗碘升华实验所用试管 | 先用酒精清洗,再用水清洗 |
C. | 测定醋酸钠溶液pH | 用玻璃棒蘸取溶液,点在湿润的pH试纸上 |
D. | 配制浓度为0.010 | 称取KMnO4固体0.158 g,放入100 mL容量瓶中,加水溶解并稀释至刻度 |
A.A B.B C.C D.D
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】25℃时,水的电离达到平衡:H2O![]() H++OH-,△H>0,下列叙述正确的是( )
H++OH-,△H>0,下列叙述正确的是( )
A. 向水中加入稀氨水,平衡逆向移动,c(OH-)降低
B. 向水中加入少量固体硫酸氢钠,c(H+)增大,Kw不变
C. 向水中加入少量固体CH3COONa,平衡逆向移动,c(H+)降低
D. 将水加热,Kw不变,pH不变
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】
化合物M是一种香料,A与D是常见的有机化工原料,按下列路线合成化合物M:
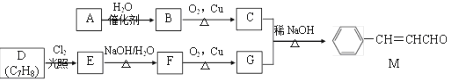
已知以下信息:
①A的相对分子质量为28

回答下列问题:
(1)A的名称是___________,A的结构简式___________。D的结构简式是___________。
(2)A生成B的反应类型为________,C中官能团名称为___________。
(3)E生成F的的化学方程式为___________。
(4)下列关于G的说法正确的是___________。(多选)
a.属于芳香烃
b.可与FeCl3溶液反应显紫色
c.可与新制的Cu(OH)2共热生成红色沉淀
d.G分子中最多有14个原子共平面
(5)化合物M的同系物N比M的相对分子质量大14,N的同分异构体中同时满足下列条件的共有________种(不考虑立体异构)。
①与化合物M含有相同的官能团;②苯环上有两个取代基③醛基与双键相连
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】重铬酸钾是一种重要的化工原料,一般由铬铁矿制备,铬铁矿的主要成分为FeO·Cr2O3,还含有硅、铝等杂质。制备流程如图所示:
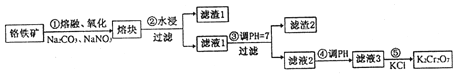
回答下列问题:
(1)步骤①的主要反应为:FeO·Cr2O3+Na2CO3+NaNO3![]() Na2CrO4+ Fe2O3+CO2+ NaNO2,上述反应配平后FeO·Cr2O3与NaNO3的系数比为__________。该步骤不能使用陶瓷容器,原因是______。
Na2CrO4+ Fe2O3+CO2+ NaNO2,上述反应配平后FeO·Cr2O3与NaNO3的系数比为__________。该步骤不能使用陶瓷容器,原因是______。
(2)滤渣1中含量最多的金属元素是_________,滤渣2的主要成分是________及含硅杂质。
(3)步骤④调滤液2的pH使之变______(填“大”或“小”),原因是______(用离子方程式表示)。
(4)某工厂用76 kg 铬铁矿粉(含Cr2O3 40%)制备K2Cr2O7,最终得到产品41.16kg,则产率为_______。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com