
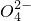 、Cl-等杂质______;
、Cl-等杂质______;| 加热前质量 | 加热前质量 | 加热后质量 |
| W1(容器) | W2(容器+晶体) | W3(容器+无水硫酸铜) |
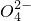 、Cl-等可溶性杂质,通常采取蒸馏的方法,故选:A;
、Cl-等可溶性杂质,通常采取蒸馏的方法,故选:A; ,
, ;
; =2.35℃,所以放出的热量Q=4.18J/(g?℃)×100g×2.35℃=4.18×100×2.35J=0.418×2.35kJ,参加反应的n(HCl)=0.05L×0.50mol?L-1=0.025mol.
=2.35℃,所以放出的热量Q=4.18J/(g?℃)×100g×2.35℃=4.18×100×2.35J=0.418×2.35kJ,参加反应的n(HCl)=0.05L×0.50mol?L-1=0.025mol.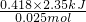 =-
=-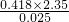 kJ/mol,故答案为:-
kJ/mol,故答案为:-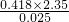 .
.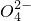 、Cl-等可溶性杂质,通常采取蒸馏的方法;
、Cl-等可溶性杂质,通常采取蒸馏的方法;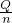 ,参加反应的n(HCl)=0.05L×0.50mol?L-1=0.025mol.
,参加反应的n(HCl)=0.05L×0.50mol?L-1=0.025mol.

科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
| 加热前质量 | 加热前质量 | 加热后质量 |
| W1(容器) | W2(容器+晶体) | W3(容器+无水硫酸铜) |
| 160(W2-W3) |
| 18(W3-W1) |
| 160(W2-W3) |
| 18(W3-W1) |
| 0.418×2.35 |
| 0.025 |
| 0.418×2.35 |
| 0.025 |
查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
A.分馏 B.盐析 C.过滤 D.重结晶
E.升华 F.渗析 G.电解 H.加热分解
I.蒸馏
下列各组混合物的分离或提纯应选用哪一种方法最合适?
(1)除去Ca(OH)2溶液中悬浮的CaCO3微粒,用___________。
(2)除去Fe(OH)3胶体中混有的Cl-离子,用___________。
(3)除去乙醇中溶解的微量食盐,用___________。
(4)分离石油中各种不同沸点范围的成分,用___________。
(5)除去固体碘中混有的少量NaI,用___________。
(6)除去氧化钙中的CaCO3___________。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com