
| A. | 能量最低原理 | B. | 能量守恒原理 | C. | 泡利原理 | D. | 洪特规则 |
分析 基态原子的核外电子排布的原则为能量最低原理、泡利不相容原理和洪特规则,据此进行解答.
解答 解:基态原子的核外电子排布的原则为能量最低原理、泡利不相容原理和洪特规则,
能量最低原理:原子核外电子先占有能量低的轨道,然后依次进入能量高的轨道;
泡利不相容原理:每个原子轨道上最多只能容纳2个自旋状态相反的电子;
洪特规则:洪特规则是在等价轨道(相同电子层、电子亚层上的各个轨道)上排布的电子将尽可能分占不同的轨道,且自旋方向相同;
所以基态原子的核外电子排布的原则不包括能量守恒原理,
故选B.
点评 本题考查了基态原子的核外电子排布的原则,题目难度不大,明确基态原子的核外电子排布的原则为解答关键,试题侧重基础知识的考查,培养了学生的灵活应用能力.


 培优三好生系列答案
培优三好生系列答案 优化作业上海科技文献出版社系列答案
优化作业上海科技文献出版社系列答案科目:高中化学 来源: 题型:实验题
查看答案和解析>>
科目:高中化学 来源: 题型:推断题
| 族 周期 | IA | 0族 | ||||||
| 1 | ① | IIA | IIIA | ⅣA | VA | ⅥA | VIIA | |
| 2 | ② | ③ | ||||||
| 3 | ④ | ⑤ | ⑥ | ⑦ | ⑧ | |||
 .
.| 序号 | 条件 | 现象 | 结论 | ||
| 温度/℃ | 催化剂 | ||||
| 第一组 | 1 | 40 | FeCl3溶液 | 快速产生大量气泡 | 相同条件下,温度升高,化学反应速率加快 |
| 2 | 20 | A | 缓慢产生适量气泡 | ||
| 3 | 5 | FeCl3溶液 | 缓慢产生极少量气泡 | ||
| 第二组 | 4 | t | MnO2 | 快速产生大量气泡 | |
| 5 | 20 | 无 | 缓慢产生极少量气泡 | ||
查看答案和解析>>
科目:高中化学 来源: 题型:解答题


查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 向硫酸氢钠溶液中滴加Ba(OH)2溶液恰好至中性:2H++SO42-+Ba2++2OH-═BaSO4↓+2H2O | |
| B. | 等物质的量浓度的FeI2溶液与溴水等体积混合:2Fe2++2I-+2Br2═2Fe3++I2+4Br- | |
| C. | 用惰性电极电解CuSO4溶液:2Cu2++2H2O$\frac{\underline{\;电解\;}}{\;}$2Cu+O2↑+4H+ | |
| D. | 硫氢化钠水解:HS-+H2O?H2S+OH- |
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
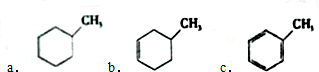
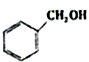 c.
c.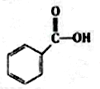
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 加入铁粉,铁粉不溶解 | B. | 滴入 NaNO3溶液,铜片溶解 | ||
| C. | 加入银粉,银粉不溶解 | D. | 滴入 NaHCO3溶液,有气体产生 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | Ba2+、Na+、CO32-、SO42- | B. | Mg2+、Cl-、Na+、SO42- | ||
| C. | K+、Cl-、HCO3-、NO3- | D. | K+、Na+、Fe2+、NO3- |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com