
������ʾ�����������ڴ����а���ȼ�ա�������ijУ��ѧС��ѧ���������(ͼ�����еȼг�װ������ȥ)���а����������ڲ�ͬ�����·�Ӧ��ʵ�顣
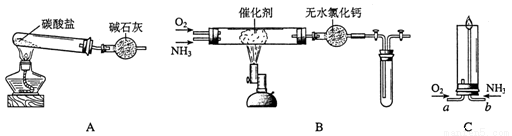
��1����װ��A��ȡ����������İ��������Թ���̼���εĻ�ѧʽ��______����ʯ�ҵ�������______��
��2���������İ��������������ͨ��װ��B������Ϊ��ʯ�ޣ��У��þƾ���Ƽ��ȣ����������Ļ�ѧ����ʽ��____________________________��
��3����������������A�����İ����ֱ��a��b���ܽ�����ͨ�뵽װ��C�У�����b���϶˵�ȼ������
��������ͨ����Ⱥ�˳����___________����������___________________��
�ڰ���ȼ�յĻ�ѧ����ʽ��________________________��
 �㽭��У��ʦ���ϵ�д�
�㽭��У��ʦ���ϵ�д� ȫ�ų��100��ϵ�д�
ȫ�ų��100��ϵ�д�
| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ��2015-2016ѧ��ɽ����ѧ������ѧ��һ�����л�ѧ�Ծ��������棩 ���ͣ�ѡ����
500mL����MgCl2��NaCl��Na2SO4�������ʵĻ����Һ����֪���к���Cl��Ϊ1.8mol��Na��Ϊ2mol��Mg2��Ϊ0.5mol����SO42-�����ʵ���Ũ��Ϊ
A��0.6mol /L B��0.7mol /L C��1.2mol /L D��1.0mol /L
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ��2015-2016ѧ���㽭��Ҧ��ѧ�߶���ѧ�����п��Ի�ѧ�Ծ��������棩 ���ͣ�ѡ����
ij��Һ����ˮ���������������Ũ��c(H+)=1��10-14 mol��L-1����������Һ����ܴ����������������
A��Al3+��NH4+��SO42-��Cl-
B��K+��Fe2+��MnO4-��Cl-
C��NH4+��SiO32-��NO3-��K+
D��Na+��K+��HCO3-��Mg2+
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ��2015-2016ѧ��ɽ����ׯ���и߶�10��ѧ����黯ѧ���������棩 ���ͣ�ѡ����
����������������
A����ѧ��Ӧ�������������ı仯
B����Ҫ���Ȳ��ܷ����ķ�Ӧ��һ�������ȷ�Ӧ
C�����ʵĻ�ѧ�ܿ�����һ��������ת��Ϊ���ܡ�����Ϊ��������
D�����ȷ�Ӧ�����ڷ�Ӧ��������С�������������������û�����ü�ֵ
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ��2015-2016ѧ�꽭���߰���ѧ��һ�����л�ѧ�����ص�ࣩ�������棩 ���ͣ������
���ݷ�Ӧ3Cu��8HNO3(ϡ)=3Cu(NO3)2��2NO����4H2O���ش��������⣺
��1����ԭ����________����ԭ������________����������________������������________��
��2����ԭ���뻹ԭ��������ʵ���֮����________��
��3������8 mol HNO3�μӷ�Ӧʱ�������������ʵ�����Ϊ________g����Ӧ��ת�Ƶĵ��ӵ����ʵ���Ϊ________ mol��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ��2015-2016ѧ��ӱ������и�һ�ϵ��Ĵ��¿���ѧ�Ծ��������棩 ���ͣ�ʵ����
ijУ��ѧ����С��Ϊ�˼���̼���ƺ�̼���������ְ�ɫ���壬�ò�ͬ�ķ�����������ʵ�飬��ͼI��IV��ʾ��

��1��ֻ����ͼI��II��ʾʵ�飬�ܹ��ﵽʵ��Ŀ�ĵ���(��װ�����)__________��
��2��ͼIII��IV��ʾʵ����ܼ������������ʣ��䷴Ӧ�Ļ�ѧ����ʽΪ___________________����ʵ��III ��ȣ�ʵ��IV���ŵ���(��ѡ�����)__________��
A�� III��IV����
B�� IV��III��ȫ
C�� IV��III�������
D�� IV����������һ��װ��ͬʱ���������Ա�ʵ�飬��III����
��3������ʵ��V��֤���ƺ�̼�����Ƶ��ȶ��ԣ����Թ�B��װ��Ĺ��������(�ѧʽ)______��
��4����̼��������Һ�����ʯ��ˮ��ϲ���ַ�Ӧ��
�ٵ�ʯ��ˮ����ʱ�������ӷ���ʽΪ___________����̼���������������Ƶ����ʵ���֮����2:1ʱ��������Һ�е����ʵĻ�ѧʽΪ______��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ��2015-2016ѧ��ӱ������и�һ�ϵ��Ĵ��¿���ѧ�Ծ��������棩 ���ͣ�ѡ����
������ԭ�Ӻ������ӣ����������������( )
A���������һ�����Ӳ� B�����ǵĻ�ѧ��������
C����ԭ�Ӱ뾶�������Ӵ� D����ԭ�ӡ������Ӿ�ΪͬһԪ��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ��2015-2016ѧ��㶫ʡ�߶������в��Ի�ѧ�Ծ��������棩 ���ͣ�ѡ����
�����Ȼ�ѧ����ʽ����д����ȷ����
A��500 �桢30 MPa�£���0.5 mol N2��1.5 mol H2�����ܱյ������г�ַ�Ӧ����NH3(g)������19.3 kJ�����Ȼ�ѧ����ʽΪ��N2 ��3H2  2NH3 ��H����38.6 kJ��mol��1
2NH3 ��H����38.6 kJ��mol��1
B����֪��105Pa�� 298K�����£�2mol H2ȼ������ˮ�����ų�484kJ�����������Ȼ�ѧ����ʽΪ��H2(g) + 1/2O2(g) == H2O(g) ��H����242 kJ��mol��1
C������ı�ȼ������ֵΪ890.3 kJ/mol�������ȼ�յ��Ȼ�ѧ����ʽΪ��CH4(g) + 2O2(g)= CO2(g) + 2H2O(g) ��H= -890.3 kJ/mol
D����֪ϡ��Һ�У�H��(aq)��OH��(aq)===H2O(l) ��H����57.3 kJ��mol��1����Ũ������ϡNaOH��Һ��Ӧ����1 molˮʱ�ų�������Ϊ57.3 kJ��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ��2016��ɽ��ʡ����12���¿���ѧ�Ծ��������棩 ���ͣ�ѡ����
���ֶ�����Ԫ����Ԫ�����ڱ��е����λ����ͼ��ʾ�����б�Ԫ������������������Ӳ�����2��������������ȷ���ǣ� ��
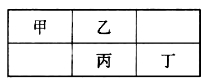
A������Ԫ�صĵ����У������ʵ��ۡ��е����
B����Ԫ���������Ӧˮ���������һ��ǿ�ڱ�
C����Ԫ���γɵĵ��������ӻ�ԭ��ǿ�ڱ�
D����Ԫ�ص����ڻ�ѧ��Ӧ��ֻ����������
�鿴�𰸺ͽ���>>
����ѧУ��ѡ - ��ϰ���б� - �����б�
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com