
| A. | 化学平衡常数是受溶液的浓度、气体的压强、体系的温度等外界条件影响的 | |
| B. | 某电解质溶液中,温度升高,Kw增大,则溶液的酸性或碱性一定增强 | |
| C. | H2CO3的电离常数表达式:K=$\frac{c({H}^{+})•c(C{O}_{3}^{2-})}{c({H}_{2}C{O}_{3})}$ | |
| D. | 电离平衡常数可以表示弱电解质的相对强弱 |
分析 A.K只与温度有关;
B.NaCl溶液中温度升高,Kw增大;
C.H2CO3为二元弱酸,分步电离;
D.Ka越大,电离程度越大,酸性越强.
解答 解:A.K只与温度有关,与溶液的浓度、气体的压强均无关,故A错误;
B.NaCl溶液中温度升高,Kw增大,而溶液为中性,故B错误;
C.H2CO3为二元弱酸,分步电离,Ka1=$\frac{c({H}^{+})•c(HC{O}_{3}^{-})}{c({H}_{2}C{O}_{3})}$,故C错误;
D.Ka越大,电离程度越大,酸性越强,则电离平衡常数可以表示弱电解质的相对强弱,故D正确;
故选D.
点评 本题考查平衡常数的意义,为高频考点,把握化学平衡常数、电离平衡常数、Kw的应用为解答的关键,侧重分析与应用能力的考查,注意K只与温度有关,题目难度不大.


科目:高中化学 来源: 题型:解答题
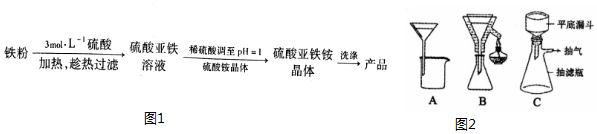
| 物质 | 0℃ | 10℃ | 20℃ | 30℃ | 40℃ | 50℃ | 70℃ |
| FeSO4•7H2O | 28.8 | 40.0 | 48.0 | 60.0 | 73.3 | - | - |
| (NH4)2SO4 | 70.6 | 73 | 75.4 | 78.0 | 81 | 84.5 | 94.9 |
| (NH4)2SO4•FeSO4•6H2O | 14.5 | 18.1 | 21.2 | 24.5 | 27.9 | 31.3 | 38.5 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 不慎将酸或碱液溅入眼内,立即闭上眼睛,用手揉擦 | |
| B. | 实验桌上的酒精灯倾倒了燃烧起来,马上用湿布扑灭 | |
| C. | 皮肤上溅有较多的浓硫酸,赶紧用水冲洗 | |
| D. | 衣服沾上大量的浓氢氧化钠溶液,需将此衣服浸泡在盛水的盆中 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
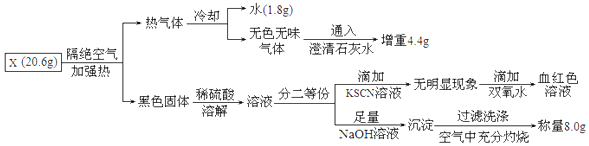
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 物质的量之比为2:1 | B. | 体积之比为1:2 | ||
| C. | 质量之比为16:7 | D. | 密度之比为7:16 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 用金属钠可区分乙醇和乙醚 | |
| B. | 用酸性高锰酸钾溶液可区分乙烷和乙烯 | |
| C. | 用水可区分苯和溴苯 | |
| D. | 用新制的银氨溶液可区分甲酸甲酯和乙醛 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | ①②⑥ | B. | ②④⑤ | C. | ②④ | D. | ⑤⑥ |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com