
【题目】设NA为阿伏加德罗常数,下列有关说法正确的是( )
A.1mol甲基(-CH3)所含的电子总数为8NA
B.0.5mol苯分子中含有C=C双键数为1.5NA
C.11.2L甲醛所含分子数为0.5NA
D.14g乙烯、丙烯的混合气体所含原子数为3NA
科目:高中化学 来源: 题型:
【题目】在溶液中加入足量Na2O2后仍能大量共存的离子组是( )
A.K+、AlO2-、Cl-、SO42-B.Ca2+、Fe2+、NO3-、HCO3-
C.NH4+、Ba2+、Cl-、NO3-D.Na+、Cl-、CO32-、SO32-
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】CoCl2· 6H2O是一种饲料营养强化剂。一种利用水钴矿(主要成分为Co2O3、 Co(OH)3,还含少量Fe2O3、Al2O3、MnO等)制取CoCl2· 6H2O的工艺流程如下:
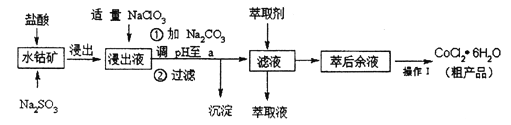
已知:①浸出液含有的阳离子主要有H+、Co2+、Fe2+、Mn2+、Al3+等;
②部分阳离子以氢氧化物形式沉淀时溶液的pH见下表(金属离子浓度为0.01 mol/L):
沉淀物 | Fe(OH)3 | Fe(OH)2 | Co (OH) 2 | Al(OH)3 | Mn(OH)2 |
开始沉淀 | 2.7 | 7.6 | 7.6 | 4.0 | 7.7 |
完全沉淀 | 3.7 | 9.6 | 9.2 | 5.2 | 9.8 |
③CoCl2· 6H2O熔点为86℃,加热至110~120℃时,失去结晶水生成无水氯化钴。
(1)写出浸出过程中主要发生的离子反应方程式:______________。
(2)若不慎向“浸出液”中加过量NaC1O3时,可能会生成的有害气体是_______(填化学式)。
(3)萃取剂对金属离子的萃取率与pH的关系如图,向“滤液”中加入萃取剂的目的是_______,其使用的最佳pH范围是 ________(选填下列字母)。

A. 2.0~2.5 B. 3.0~3.5 C. 4.0~4.5 D. 5.0~5.5
(4) “操作1”是________。制得的CoCl2· 6H2O需减压烘干的原因是__________。
(5)为测定粗产品中CoCl2· 6H2O的含量,称取一定质量的粗产品溶于水,加入足量AgNO3溶液,过滤、洗涤,将沉淀烘干后称其质量。通过计算发现粗产品中CoCl2· 6H2O的质量分数大于100%,其原因可能是___________________。(答一条即可)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列有关实验的操作或叙述正确的是

A.可用如图装置检验火柴头燃烧是否产生SO2
B.纸层析法分离含有少量Cu2+和Fe3+的混合溶液时,亲水性强的Cu2+在滤纸下方
C.取某试样溶液少量,加入苯酚,同时再加入氯水,若溶液显紫色,说明原试样中含Fe2+
D.取出分液漏斗中所需的上层液体:下层液体从分液漏斗下端管口流出后,及时关闭活塞,然后更换一个接收容器,打开活塞将分液漏斗中的液体放出
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】现有甲、乙、丙、丁四个装置,下列有关说法不正确的是

A.选用合适的试剂,使用甲装置在实验室可以制备少量H2、O2、CO2、Cl2、NO2、NH3
B.采用不同的通气方法,使用乙装置可收集H2、NH3、CO、NO、SO2、O2、Cl2
C.选用丙装置处理尾气,可以吸收Cl2、SO2、H2S、NO2、HCl
D.选用丁装置可以净化NH3(H2O)、O2(CO2)、H2(HCl)(括号内为杂质气体)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列叙述正确的是( )
A.在同温同压下,甲容器中的氧气(O2)和乙容器中的氨气(NH3)所含的原子个数相同,则甲、乙两容器中气体的体积之比为1:2
B.任何条件下,等物质的量的甲烷(CH4)和一氧化碳所含的原子数一定相等
C.在标准状况时,20mL NH3与60mL N2所含的原子个数比为1:3
D.同温同压下,1L一氧化碳气体一定比1L氧气的质量小
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列事实中能用平衡移动原理解释的是
A. 使用催化剂可加快氨的合成速率
B. 在FeSO4溶液中,加入铁粉以防止氧化
C. 由H2蒸气、I2蒸气、HI组成的平衡体系加压后颜色变深
D. 硫酸工业生产中,通入过量空气以提高SO2的利用率
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】I.已知:
①2H2(g)+O2(g)=2H2O(g) △H=-483.6kJ/mol
②H2O(l)= H2O(g) △H=+44kJ/mol
③C(s)+ ![]() O2(g)=CO(g) △H=-110.5kJ/mol
O2(g)=CO(g) △H=-110.5kJ/mol
④C(s)+O2(g)=CO2(g) △H=-393.5kJ/mol
回答下列问题:
(1)上述变化中吸热的是___________。
(2)C的燃烧热△H=___________。
(3)燃烧2gH2生成液态水,放出的热量为___________。
(4)写出CO燃烧的热化学方程式___________。
Ⅱ.在一定条件下,xA+yB![]() zC可逆反应达到平衡,试填出:
zC可逆反应达到平衡,试填出:
(1)若A、B、C都是气体,在减压后平衡向逆反应方向移动,则x、y、z的关系是_______。
(2)若C是气体,并且x+y=z,在加压时化学平衡如发生移动必定向_______。(填正或逆)反应方向移动。
(3)当改变某种反应条件后,正反应速率增大,而气体A和气体B的浓度均未变,则改变的条件可能是_______。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com