
A.电路中通过电子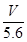 mol mol | B.n= |
C.溶液中H+增加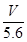 mol mol | D.n=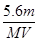 |
 备战中考寒假系列答案
备战中考寒假系列答案科目:高中化学 来源:不详 题型:单选题
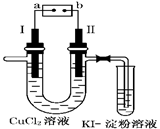
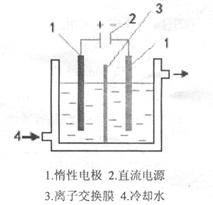
| A.电源a极为负极 |
| B.KI—淀粉溶液会变蓝色 |
| C.若加入适量CuCl2可使电解后的溶液恢复原状态 |
| D.电极Ⅰ上发生的电极反应为:Cu-2e-=Cu2+ |
查看答案和解析>>
科目:高中化学 来源:不详 题型:填空题

 沉淀完全,而在pH≥3.2时
沉淀完全,而在pH≥3.2时
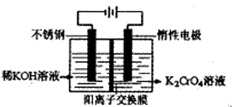
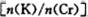 为d,则此时的铬酸钾的转化率为 。
为d,则此时的铬酸钾的转化率为 。查看答案和解析>>
科目:高中化学 来源:不详 题型:实验题
 6Cu+SO2↑,反应的氧化剂是 。
6Cu+SO2↑,反应的氧化剂是 。
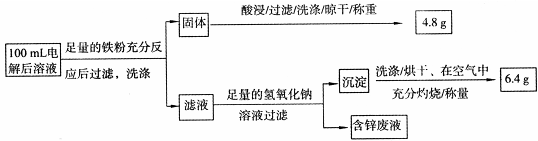
查看答案和解析>>
科目:高中化学 来源:不详 题型:实验题
| 实验操作 | 现象及结论 |
| | |
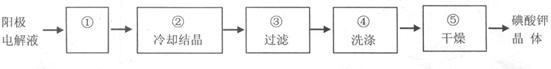
查看答案和解析>>
科目:高中化学 来源:不详 题型:填空题
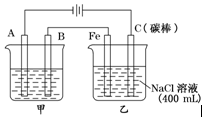
查看答案和解析>>
科目:高中化学 来源:不详 题型:计算题
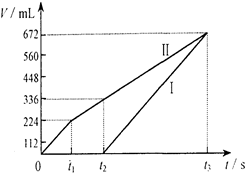
查看答案和解析>>
科目:高中化学 来源:不详 题型:填空题

查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| A.阴极自始自终只析出H2 | B.阳极先析出Cl2,后析出O2 |
| C.电解最后阶段为电解水 | D.溶液PH值不断增大,最后为7 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com