
【题目】设NA为阿伏加德罗常数的值。下列说法不正确的是( )
A. 常温常压下,8 g O2含有4NA个电子
B. 盛有SO2的密闭容器中含有NA个氧原子,则SO2的物质的量为0.5 mol
C. 常温常压下,14 g由N2与CO组成的混合气体含有的原子数目为2NA
D. 标准状况下,22.4 L的NO2和CO2混合气体含有2NA个O原子
 阅读快车系列答案
阅读快车系列答案科目:高中化学 来源: 题型:
【题目】向50mLNa2SO4和Na2CO3的混合溶液中加入过量的BaCl2溶液,得到14.51g白色沉淀,向白色沉淀中加入过量的稀HNO3,充分反应后,沉淀减少到4.66g,并有气体产生。
(1)原混合溶液中Na2SO4的物质的量浓度是______________。
(2)产生的气体在标准状况下的体积是______________。
(3)原溶液中Na+物质的量浓度是______________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】生物界与非生物界具有统一性,是因为
A. 构成细胞的化合物在非生物界都存在
B. 构成细胞的无机物在非生物界都存在
C. 构成细胞的化学元素在非生物界都存在
D. 生物与非生物都具有新陈代谢的功能
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】据估计,地球上的绿色植物通过光合作用每年能结合来自CO2中的碳1500亿吨和来自水中的氢250亿吨,并释放4000亿吨氧气。光合作用的过程一般可用下式表示:

CO2+H2O+微量元素(P、N等)![]() (蛋白质、碳水化合物、脂肪等)+O2
(蛋白质、碳水化合物、脂肪等)+O2
下列说法不正确的是
A. 某些无机物通过光合作用可转化为有机物
B. 碳水化合物就是碳和水组成的化合物
C. 叶绿素是光合作用的催化剂
D. 增加植被,保护环境是人类生存的需要
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】利用电解法可将含有Fe、Zn、Ag、Pt等杂质的粗铜提纯,下列叙述正确的是( )
A. 电解时以精铜作阳极
B. 电解时阴极发生氧化反应
C. 粗铜连接电源负极,其电极反应是Cu-2e-===Cu2+
D. 电解后,电解槽底部会形成含少量Ag、Pt等金属的阳极泥
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】工业上常用SiO2与C在高温下发生反应制造粗硅,粗硅中含有SiC,其中Si和SiC的物质的量之比为1∶1。下列说法正确的是( )
A.硅元素在地壳中含量居第二位,主要以单质硅和硅酸盐的形式存在
B.纯净的SiO2只能用于制造光导纤维
C.SiC因有很高的化学稳定性和热稳定性,故可用作高温结构陶瓷材料。
D.制造粗硅时的上述反应方程式为:2SiO2+5C![]() Si+SiC+4CO↑
Si+SiC+4CO↑
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】已知A、B、C、D、E、F、G、H、I均为有机物,根据下列框图和已知条件回答问题:

已知:A中有一个甲基,D都能使溴水褪色,F能发生银镜反应,I的结构简式为: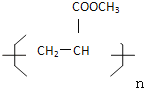
请回答下列问题:
(1)A中含有的官能团: (文字叙述)
(2)属于取代反应的有:
(3)写出反应④的化学方程式
(4)写出A的结构简式
(5)E有多种同分异构体,其中一种既能发生银镜反应又能和NaOH溶液反应,请写出它的结构简式
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】36.5 g HCl溶解在1 L水中(水的密度近似为1 g/cm3),所得溶液的密度为ρg/cm3,质量分数为ω,物质的量浓度为cmol/L,NA表示阿伏加德罗常数,则下列叙述中正确的是( )
A. 所得溶液的物质的量浓度:c=1 mol/L
B. 所得溶液中含有NA个HCl分子
C. 36.5 g HCl气体占有的体积为22.4 L
D. 所得溶液的质量分数:ω=36.5c/1 000ρ
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】
硫酸
分子式:H2SO4
相对分子质量:98
密度:1.84g/mL
H2SO4的质量分数:98%
(1)该浓硫酸中H2SO4的物质的量浓度为 。
(2)某学生欲用上述浓硫酸和蒸馏水配制250mL物质的量浓度为0.4 mol·L-1的稀硫酸,该学生需要量取 mL上述浓硫酸进行配制。
(3)为配制(2)中的稀硫酸,下列可供选用的仪器中,一定用到的是 (填编号),配制过程中还缺少的仪器是 。(填写仪器名称)
①玻璃棒; ②胶头滴管;③量筒;④药匙;⑤圆底烧瓶;⑥天平;⑦烧杯;⑧普通漏斗
(4)在配制过程中,下列实验操作可能导致配制的硫酸溶液浓度偏高的是 (填序号)。
①定容时俯视观察
②定容后经振荡、摇匀、静置后,发现液面下降,再加适量的蒸馏水
③浓硫酸在烧杯中加水稀释后,未冷却就向容量瓶中转移
④容量瓶使用时未干燥
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com