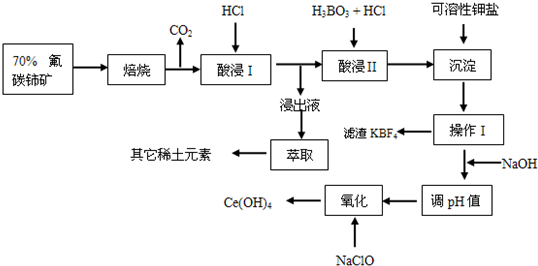
解:(1)对于固体参加的反应来说,固体表面积越大,反应速率越大,故答案为:增大固体与空气的接触面积,增大反应速率;提高原料的利用率;
(2)根据题意可知应为KBF4沉淀,故答案为:K++BF4-=KBF4↓;
(3)在生产过程中,酸浸I中会产生大量黄绿色气体,说明Ce4+离子具有强氧化性,可将Cl-氧化为Cl2,为避免污染环境、腐蚀设备,应用硫酸酸浸,故答案为:2Ce4++2Cl-=2Ce3++Cl2↑;用H2SO4酸浸;
(4)过滤用到的仪器有铁架台、烧杯、漏斗、玻璃棒和滤纸等;实验室测定PH的方法是撕下一小片pH试纸放在干燥洁净的表面皿上,用玻璃棒蘸取该溶液点在pH试纸的中央,然后与标准比色卡对比;故答案为:漏斗、烧杯、玻璃棒;撕下一小片pH试纸放在干燥洁净的表面皿上,用玻璃棒蘸取该溶液点在pH试纸的中央,然后与标准比色卡对比;
(5)NaClO将Ce(OH)3氧化为Ce(OH)4,其中NaCl为还原产物,故答案为:2Ce(OH)3+NaClO+H2O=2Ce(OH)4+NaCl;
NaCl.
分析:(1)影响化学反应速率的因素有浓度、温度、压强、催化剂以及表面积等因素,对于固体参加的反应来说,固体表面积越大,反应速率越大;
(2)根据题意及元素守恒来判断可知应为KBF4沉淀;
(3)在生产过程中,酸浸I中会产生大量黄绿色气体,说明Ce4+离子具有强氧化性,可将Cl-氧化为Cl2,
(4)过滤是将固体和液体化合物分离的一种提纯方法,用到的仪器有铁架台、烧杯、漏斗、玻璃棒和滤纸等;实验室测定PH的方法是撕下一小片pH试纸放在干燥洁净的表面皿上,用玻璃棒蘸取该溶液点在pH试纸的中央,然后与标准比色卡对比;
(5)由题目中“酸浸I的浸出液中含少量的+3价的铈”可知,加入NaOH后生成Ce(OH)3,NaClO将Ce(OH)3氧化为
Ce(OH)4.
点评:本题既有常规知识的考查又有新情景题目的考查,常规题目涉及到影响化学反应速率的因素、过滤操作以及PH的测定方法;命题情景要求根据题意写出有关反应的方程式,做题时注意根据物质的性质正确判断反应物和生成物,用守恒的方法去书写.



 名校课堂系列答案
名校课堂系列答案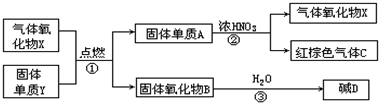 X,Y,A,B,C,D是中学化学教材中常见的物质,且有图示的转化关系.气体C的式量比气体X的式量大2,D的焰色反应呈黄色,产物中水已忽略.
X,Y,A,B,C,D是中学化学教材中常见的物质,且有图示的转化关系.气体C的式量比气体X的式量大2,D的焰色反应呈黄色,产物中水已忽略.