
��ֻ�Լ�ƿ�зֱ�ʢ��NaNO3��Һ��Na2CO3��Һ��Na2SO4��Һ��NaCl��Һ�������ڼ�����Լ���Ba(NO3)2��Һ��AgNO3��Һ��ϡHNO3������μ�����������Һ�ֱ�ش����и��⡣����֧�Թ��зֱ�ȡ������Һ��1mL����һ����ʵ��˳���������ʵ�顣
��1������֧�Թ��зֱ����___________�����ֵ�������____________������ȷ���Թ��е���Һ��___________���ӷ���ʽ��_____________________________________��
��2����ʣ����֧�Թ��зֱ����___________�����ֵ�������_________������ȷ���Թ��е���Һ��___________���ӷ���ʽ��_____________________________________��
��3����ʣ����֧�Թ��зֱ����___________�����ֵ�������__________������ȷ���Թ��е���Һ��___________���ӷ���ʽ��_____________________________________��
��4������ʵ���ж�û�����Ա仯����_______________��
 ��ѧ����ͬ����ϰϵ�д�
��ѧ����ͬ����ϰϵ�д� ��ǰ�κ�ͬ����ϰϵ�д�
��ǰ�κ�ͬ����ϰϵ�д�
| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ��2015-2016ѧ�꺣��ʡ�߶������У�������ѧ�Ծ��������棩 ���ͣ������
��һ���¶��£���2.4molA��1.2molB�����������Ϻ����ݻ�Ϊ2L��ij�ܱ������У��������·�ӦA(g)+B(g)  x C(g)+D(g) ��H<0��2minĩ��Ӧ�ﵽƽ��״̬��������0.8molD�������C��Ũ��Ϊ0.4mol/L������д���пհף�
x C(g)+D(g) ��H<0��2minĩ��Ӧ�ﵽƽ��״̬��������0.8molD�������C��Ũ��Ϊ0.4mol/L������д���пհף�
��1��xֵ����________________ 2min��v(B)= ��
��2��A��ת����Ϊ_________________��
��3���÷�Ӧ�ﵽƽ��ʱ�����������м���1.2molA��0.6molB���ٴδﵽƽ���A��ת���� �����������С�����䡱�� ��
��4���÷�Ӧ��ƽ�ⳣ���ı���ʽk = ��450��ʱƽ�ⳣ��_____________500��ʱƽ�ⳣ��������ڡ�����С�ڡ����ڡ��� ��
��5����ͬ�¶��£�����ʼʱ��������г���0.4 mol A��0.4 mol B��0.2molC��0.2molD����Ӧ�ﵽƽ��ǰ����Ӧ����v�� v�棨�>�� �� ��<�������ﵽƽ��ʱD��Ũ��Ϊ ��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ��2015-2016ѧ�����ɹŰ�ͷ���и�һ��12���¿���ѧ�Ծ��������棩 ���ͣ�ѡ����
��ͭ�����Ҫ�ɷ���Cu2O����ͭ�����Ҫ�ɷ���Cu2S������ͭ�����ͭ���ϼ��ȷ������·�Ӧ��Cu2S+2Cu2O��6Cu+SO2�������ڸ÷�Ӧ��˵���У���ȷ����
A���÷�Ӧ��������ֻ��Cu2O
B��Cu2S�ڷ�Ӧ�м��������������ǻ�ԭ��
C��Cu���������������ǻ�ԭ����
D��ÿ����19.2g Cu����Ӧ��ת��0.6 mol����
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ��2015-2016ѧ����������ɽ��ѧ�߶��ϵڶ����¿���ѧ�Ծ��������棩 ���ͣ�ѡ����
������pH=2����������ҺA��B���ֱ��ˮϡ��1000������pHֵ������ˮ������仯��ͼ��ʾ�����н�����ȷ����
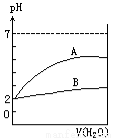
A����B����A�ĵ���ȴ�
B��AΪ���ᣬBΪǿ��
C����B�����ʵ���Ũ�ȱ�A��С
D��A���B������
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ��2015-2016ѧ����������ɽ��ѧ�߶��ϵڶ����¿���ѧ�Ծ��������棩 ���ͣ�ѡ����
���й��ڵ���ƽ�ⳣ����K����˵������ȷ����
A����һ���¶ȣ���ͬŨ��ʱ����ƽ�ⳣ����K��Խ����Ա�ʾ������ʵ���̶�Խ��
B������ƽ�ⳣ����K�����¶���
C����ͬŨ�ȵ�ͬһ������ʣ������ƽ�ⳣ����K����ͬ
D����Ԫ�����������ƽ�ⳣ�����ϵΪK1<K2<K3
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ��2015-2016ѧ��ɽ��ʡ��һ��11���¿���ѧ�Ծ��������棩 ���ͣ�ѡ����
��9.58 g Na2CO3��10H2O��NaHCO3�Ļ��������ˮ���100mL��Һ�����c(Na+)=1 mol/L����ȡͬ�����Ļ�����ּ�������������ʱ�����ù��������Ϊ
A��5.30g B��7.78g C��6.72g D��6g
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ��2015-2016ѧ��ɽ��ʡ��һ��11���¿���ѧ�Ծ��������棩 ���ͣ�ѡ����
����ʵ�����ģ������������ޣ��������Ӧʵ���һ����
ѡ�� | ʵ�����ģ�ʡ�Լг�װ�ã� | ��Ӧʵ�� |
A | �ձ����������������� | CuSO4��Һ��Ũ���ᾧ |
B | �ձ�������������ͷ�ιܡ���ֽ | �������ȥBaSO4�е�����BaCO3 |
C | �ձ�������������ͷ�ιܡ�����ƿ | �ù���BaCl2����0.5mol��L��1����Һ |
D | �ձ�������������ͷ�ιܡ���Һ©�� | ����ˮ��CCl4��ȥNaBr��Һ��������NaI ����ʾ��Br2��2NaI=2NaBr��I2�� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ��2015-2016ѧ��ɽ��ʡ��һ��12���¿���ѧ�Ծ��������棩 ���ͣ�ѡ����
��FeCl3��CuCl2�Ļ����Һ�м������ۣ���ַ�Ӧ�����й�����ڣ��������жϲ���ȷ����
A������KSCN��Һһ�������ɫ B����Һ��һ������Fe2+
C����Һ��һ������Cu2+ D��ʣ�������һ������Cu
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ��2016������ʡ������ѧ��12���¿���ѧ�Ծ��������棩 ���ͣ�ѡ����
�������ʵ�ת������ͨ��һ����Ӧʵ�ֵ���
A��NaAlO2��Al(OH)3��Al
B��N2��NO2��HNO3
C��NaOH��Na2CO3��NaHCO3
D��FeS2��SO3��H2SO4
�鿴�𰸺ͽ���>>
����ѧУ��ѡ - ��ϰ���б� - �����б�
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com