
| A. | 原混合气体中 O2 和CH4 体积比为2:1 | |
| B. | 原混合气体中 O2 和CH4 体积比为1:1 | |
| C. | 残留固体中只有Na2CO3 | |
| D. | 残留固体中只有Na2CO3 和NaOH |
分析 反应结束后,容器内于150℃时压强约为0,说明容器中无气体,且将残留物溶于水中无气体放出,说明过氧化钠也完全反应,故容器内剩余固体为Na2CO3和NaOH,根据甲烷的组成利用C、H原子守恒可知可知生成的Na2CO3和NaOH物质的量之比为1:4,再根据反应的总化学方程式判断原混合物中甲烷、氧气的物质的量之比.
解答 解:反应后压强为0,说明容器中无气体,且将残留物溶于水中无气体放出,说明过氧化钠也完全反应,故容器内剩余固体为Na2CO3和NaOH,故D正确;
根据甲烷的组成利用C、H原子守恒可知可知生成的Na2CO3和NaOH物质的量之比为1:4,则反应的总化学方程式可写为:2CH4+O2+6Na2O2=2Na2CO3+8NaOH,所以原混合气体中O2、CH4的物质的量之比为1:2,故A、B错误;
故选D.
点评 本题考查混合物的计算,题目难度中等,关键是判断剩余固体为Na2CO3和NaOH,利用甲烷的组成确定二者物质的量之比,再利用总方程式解答可以省去中间反应复杂计算的过程.


 中考解读考点精练系列答案
中考解读考点精练系列答案科目:高中化学 来源: 题型:选择题
| A. | 红棕色的NO2加压后颜色先变深再变浅 | |
| B. | H2、I2、HI混合气体加压后颜色变深 | |
| C. | 合成氨时高温、高压对合成氨有利 | |
| D. | 醋酸溶液稀释时,溶液pH增大 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题

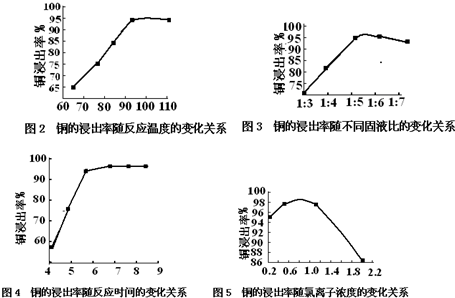
| 反应温度/℃ | 固液比 | c(Cl-)/mol•L-1 | 反应时间/h | |
| A | 95 | 1:5.5 | 0.8 | 6 |
| B | 100 | 1:5.5 | 0.7 | 7 |
| C | 110 | 1:6 | 0.9 | 8 |
| 滴定次数 | 待测溶液的体积/mL | 标准溶液的体积 | |
| 滴定前刻度/mL | 滴定后刻度/mL | ||
| 1 | 25.00mL | 0.02 | 40.01 |
| 2 | 25.00mL | 0.70 | 40.71 |
| 3 | 25.00mL | 0.20 | 39.20 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
 A、B、C、D、E、F是中学中常见的物质,其转化关系如图所示(反应条件未标出),已知反应①是置换反应.
A、B、C、D、E、F是中学中常见的物质,其转化关系如图所示(反应条件未标出),已知反应①是置换反应. ,反应③的化学方程式为4NH3+5O2$\frac{\underline{催化剂}}{△}$4NO+6H2O.
,反应③的化学方程式为4NH3+5O2$\frac{\underline{催化剂}}{△}$4NO+6H2O.查看答案和解析>>
科目:高中化学 来源: 题型:解答题
 某学习小组依据SO2具有还原性,推测SO2能被Cl2氧化生成SO2Cl2.查阅资料:SO2Cl2在常温下为无色液体,极易水解,遇潮湿空气会产生白雾.
某学习小组依据SO2具有还原性,推测SO2能被Cl2氧化生成SO2Cl2.查阅资料:SO2Cl2在常温下为无色液体,极易水解,遇潮湿空气会产生白雾.查看答案和解析>>
科目:高中化学 来源: 题型:解答题
 Na2S2O3是重要的化工原料,易溶于水,在中性或碱性环境中稳定.
Na2S2O3是重要的化工原料,易溶于水,在中性或碱性环境中稳定.查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 水电离出的C(H+)=10-13mol/L的溶液中K+、NO3-、Br-、Cl- | |
| B. | 含有大量NO3-的水溶液:I-、Fe3+、H+、Na+ | |
| C. | 弱碱性溶液中HCO3-、NH4+、C2H5O-、MnO4- | |
| D. | 无色透明溶液中:Ba2+、S2-、Cu2+、AlO2- |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com