
���� �ٻ�����м�������ˮ��һ��ɫ����Һ��˵��������в���CuCl2�������ʼ䲻�����ɳ�����
��������Һ�еμ�BaCl2��Һ�а�ɫ����������˵����Һ�к�����������ӻ�̼������ӣ�
��������ɫ����������ʱ�����������ܽ⣬�����Ϊ���ᱵ��̼�ᱵ�����Ի�����к���K2SO4��Na2CO3��̼���ƺ��Ȼ��Ʒ�Ӧ���ɳ��������������ˮ�õ���������Һ��˵����Һ����CaCl2��
����һ����Һ�м���ˮ��CCl4���ã�CCl4��dz����ɫ��Ϊ��������ɫ��˵��������в���KI��
������һ����Һ�м�AgNO3��Һ�а�ɫ�����������ó���������ϡHNO3����Һ�к��������ӣ���Ϊ������Ȼ����к��������ӣ����Բ���˵��ԭ����������Ƿ���KCl������ʵ���������ж��Ƿ���NaNO3���Դ˽����⣮
��� �⣺�ٻ�����м�������ˮ��һ��ɫ����Һ��˵��������в���CuCl2�������ʼ䲻�����ɳ�����
��������Һ�еμ�BaCl2��Һ�а�ɫ����������˵����Һ�к�����������ӻ�̼������ӣ�
��������ɫ����������ʱ�����������ܽ⣬�����Ϊ���ᱵ��̼�ᱵ�����Ի�����к���K2SO4��Na2CO3��̼���ƺ��Ȼ��Ʒ�Ӧ���ɳ��������������ˮ�õ���������Һ��˵����Һ����CaCl2��
����һ����Һ�м���ˮ��CCl4���ã�CCl4��dz����ɫ��Ϊ��������ɫ��˵��������в���KI��
������һ����Һ�м�AgNO3��Һ�а�ɫ�����������ó���������ϡHNO3����Һ�к��������ӣ���Ϊ������Ȼ����к��������ӣ����Բ���˵��ԭ����������Ƿ���KCl������ʵ���������ж��Ƿ���NaNO3��
��1��ͨ�����Ϸ���֪���϶����ڵ�������K2SO4��Na2CO3���϶������ڵ�������KI��CuCl2��CaCl2���ʴ�Ϊ��K2SO4��Na2CO3��KI��CuCl2��CaCl2��
��2�������漰��ӦΪBa2++SO42-�TBaSO4����Ba2++CO32-�TBaCO3����
����̼�ᱵ�����ᷴӦ�����Ȼ�����������̼��ˮ�����ӷ�Ӧ����ʽΪ��BaCO3+2H+=Ba2++H2O+CO2����
���漰��ӦΪAg++Cl-�TAgCl����
�ʴ�Ϊ��Ba2++SO42-�TBaSO4����Ba2++CO32-�TBaCO3����BaCO3+2H+�TBa2++CO2��+H2O��Ag++Cl-�TAgCl����
���� ���⿼���������ƶϣ�����������Һ��ɫ�����ʼ�ķ�Ӧ��֪ʶ�������������ȷ���ʵ������ǽⱾ��ؼ���ע����������Լ����������ӣ���ԭ����������Ƿ��������Ӳ���Ӱ�죬�������ж�ԭ����������Ƿ��������ӣ�Ϊ�״��㣮



| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | ���³�ѹ�£�16g O3������ԭ����ΪNA | |
| B�� | ��״���£�11.2 L NO��11.2 L O2��Ϻ�����ķ�������ΪNA | |
| C�� | �����£�pH=2��ϡ�����������е�H+����������0.01 NA | |
| D�� | ���������£�20mL 10 mol/L Ũ����������ͭ��Ӧת�Ƶ���������0.2NA |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | ������ˮ�еμ�0.1mol/L��NaOH��Һ��c��H+��+c��Na+ ��=2c��ClO-��+c��HClO��+c��OH-�� | |
| B�� | ��20mL 0.2mol/L ��H2S��Һ����μ���0.2mol/L��NaOH��Һ30mL����Һ�д������¹�ϵ��c��S2-��+2c��OH-��=c��HS-��+2c��H+��+2c��H2S�� | |
| C�� | pH��ͬ�Ģ�CH3COONa��NaClO ������Һ��c��Na+�����٣��� | |
| D�� | �����£���20mL 0.1mol/L��CH3COONa��Һ����μ���0.1mol/L������Һ��pH=7ʱ��c��CH3COOH��=c��Cl-����c��OH-��=c��H+�� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | ��ɫ��Һ�У�Na+��Cl-��SO42-��Fe3+ | |
| B�� | ��ǿ���Ե���Һ�У�Na+��SO42-��Cl-��NH4+ | |
| C�� | ʹ��ɫʯ����Һ������Һ�У�Na+��Mg2+��CO32-��Cl- | |
| D�� | ��SO42-��ˮ��Һ�У�K+��Ba2+��Cl-��Br- |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | 2g | B�� | 3g | C�� | 3.5g | D�� | 4.5g |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | Ư�ۡ���������Һ���������ǻ���� | |
| B�� | ����ͨ�����Ϸ�Ӧ�Ƶ�FeCl2��Fe��OH��3 | |
| C�� | �����������о���ȼ�գ���������ˮ������ȼ�� | |
| D�� | ��ǿ������װ����������Թܣ�������ˮ���У����ռ����������� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | 2-������ | B�� | 3��3-�������� | ||
| C�� | 3-��-2-�һ����� | D�� | 2��3��3-�������� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
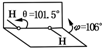 �ҹ���ѧ��¬�����뷨����ô��ѧ��Gignere������������أ�H2NCONH2����H2O2�γɼӺ���H2NCONH2•H2O2������ʹH2O2�ȶ����������ҽṹҲû�з����ı䣬�õ��˿ɹ�������ʵ��ĵ����壬���ⶨH2O2�ṹ��ͼ��ʾ�����������Ϣ���йع��������˵������ȷ���ǣ�������
�ҹ���ѧ��¬�����뷨����ô��ѧ��Gignere������������أ�H2NCONH2����H2O2�γɼӺ���H2NCONH2•H2O2������ʹH2O2�ȶ����������ҽṹҲû�з����ı䣬�õ��˿ɹ�������ʵ��ĵ����壬���ⶨH2O2�ṹ��ͼ��ʾ�����������Ϣ���йع��������˵������ȷ���ǣ�������| A�� | H2NCONH2��H2O2��ͨ�������ϵ� | B�� | H2O2�Ǽ��Է��� | ||
| C�� | H2O2�������������л�ԭ�� | D�� | H2NCONH2•H2O2�������ӻ����� |
�鿴�𰸺ͽ���>>
����ѧУ��ѡ - ��ϰ���б� - �����б�
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com