
【题目】下列叙述正确的是( )
A. 反应的活化能越小,单位时间内有效碰撞越多 B. 反应的活化能越大,单位时间内有效碰撞越多
C. 反应的活化能越小,单位时间内有效碰撞越少 D. 反应的活化能太小,单位时间内几乎无有效碰撞
 计算高手系列答案
计算高手系列答案科目:高中化学 来源: 题型:
【题目】青蒿素人工合成的部分反应流程如下:

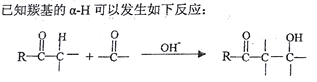
(1)化合物G中含有的官能团名称为:__________、__________,E→F的反应类型为__________。
(2)D→E先后由加成和消去两步反应完成,加成后得到的中间产物的结构简式为__________。
(3)B→C的方程式为__________。(4)写出符合下列要求的H的一种同分异构体的结构简式__________。
①既能与NaHCO3反应放出气体,也能使FeCl3溶液显紫色;
②分子中有四种不同环境的氢原子。
(5)利用题中所给信息,试以苯甲醇( )和乙烯为原料(其他无机试剂任选),合成
)和乙烯为原料(其他无机试剂任选),合成 。__________________________
。__________________________
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】锂锰电池的体积小,性能优良,是常用的一次电池。该电池反应原理如图所示,其中电解质LiClO4溶于混合有机溶剂中,Li+ 通过电解质迁移入MnO2晶格中,生成LiMnO2。
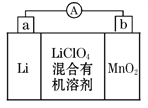
回答下列问题:
(1)外电路的电流方向是由__________极流向__________极。(填字母)
(2)电池正极反应式为________________________________________。
(3)是否可用水代替电池中的混合有机溶剂?_______(填“是”或“否”);原因是____________________________________________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】已知1.505×1023个X气体分子的质量为8 g,则X气体的摩尔质量是
A. 16 g B. 32 g C. 64 g/mol D. 32 g /mol
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】对硫-氮化合物的研究是现代无机化学最为活跃的领域之一,下图是已经合成的最著名的硫-氮化合物的分子结构。下列关于该物质说法正确的是
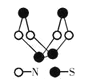
A.分子式为SN
B.分子中所有共价键的键长一定相等
C.该物质与化合物S2N2互为同素异形体
D.分子中既有极性键又有非极性键
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下表中的实线表示元素周期表的部分边界,a-1分别表示周期表中对应位置的元素。

(1)请在上表中用实线补全元素周期表边界____。
(2)表中所列元素,不属于短周期元素有____,不属于主族元素的有___(填相应的元素符号)
(3)指出下列元素在周期表中的位置:
①b元素位于第___周期___族;
②g元素位于第___周期___族;
③i元素位于第___周期___族;
(4)①写出b与c的化合物(温室气体)电子式:___________;
②用电子式表示k与h化合物形成过程:__________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】芦笋中的天冬酰胺(结构如右图)和微量元素硒、铬锰等,具有提高身体免疫力的功效。
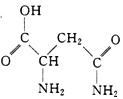
(1)天冬酰胺所含元素中, (填元素名称)元素基态原子核外未成对电子数最多。
(2)天冬酰胺中碳原子的杂化轨道类型有 种。
(3)H2S和H2Se的参数对比见下表。
化学式 | 键长/nm | 键角 | 沸点/℃ |
H2S | 1.34 | 92.3 | -60.75 |
H2Se | 1.47 | 91.0 | -41.50 |
①H2Se的晶体类型为 ,含有的共价键类型为 。
②H2S的键角大于H2Se的原因可能为 。
(4)已知铝(Mo)位于第五周期VIB族,钼、铬、锰的部分电离能如下表所示
编号 | I5/KJ·mol-1 | I6/KJ·mol-1 | I7/KJ·mol-1 | I8/KJ·mol-1 |
A | 6990 | 9220 | 11500 | 18770 |
B | 6702 | 8745 | 15455 | 17820 |
C | 5257 | 6641 | 12125 | 13860 |
A是 (填元素符号),B的价电子排布式为 。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】【2015浙江理综化学】Ⅰ.请回答:
(1)H2O2的电子式___________。
(2)镁燃烧不能用CO2灭火,用化学方程式表示其理由________________。
(3)在AgCl沉淀中加入KBr溶液,白色沉淀转化为淡黄色沉淀,写出反应的离子方程式_____________。
(4)完成以下氧化还原反应的离子方程式:
( )MnO4-+( )C2O42-+______=( )Mn2++( )CO2↑+________
Ⅱ.化合物甲和NaAlH4都是重要的还原剂。一定条件下金属钠和H2反应生成甲。甲与水反应可产生H2,甲与AlCl3反应可得到NaAlH4。将4.80g甲加热至完全分解,得到金属钠和2.24 L(已折算成标准状况)的H2。
请推测并回答:
(1)甲的化学式__________。
(2)甲与AlCl3反应得到NaAlH4的化学方程式__________。
(3)NaAlH4与水发生氧化还原反应的化学方程式__________。
(4)甲在无水条件下可作为某些钢铁制品的脱锈剂(铁锈的成分表示为Fe2O3),脱锈过程发生反应的化学方程式 。
(5)某同学认为:用惰性气体赶尽反应体系中的空气,将铁和盐酸反应后的气体经浓硫酸干燥,再与金属钠反应,得到固体物质即为纯净的甲;取该固体物质与水反应,若能产生H2,即可证明得到的甲一定是纯净的。
判断该同学设想的制备和验纯方法的合理性并说明理由___________。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com