
【题目】工业上利用硫酸废渣(含Fe2+、Fe3+的硫酸盐及少量CaO和MgO)制备高档颜料铁红(Fe2O3)并回收(NH4)2SO4,具体生产流程如图所示:
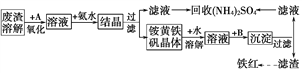
注:铵黄铁矾的化学式为(NH4)2Fe6(SO4)4(OH)12
回答下列问题:
(1)在废渣溶解操作中,加速废渣溶解的措施有________。
(2)物质A是一种氧化剂。
①工业上物质A最好选用________(填序号)。
A.空气 B.Cl2 C.MnO2 D.KMnO4
②简述工业上这样选择A的理由:__________________________________。
③写出A参与反应的离子方程式:__________________________________。
(3)往铵黄铁矾溶液(含Fe3+)中加入溶液B至pH为5时产生沉淀,请写出产生沉淀的离子方程式:__________________________________。
(4)回收所得的(NH4)2SO4晶体中可能含有的杂质是_______________________。
【答案】 不断搅拌、将废渣粉碎、升高温度(其他合理答案均可) A 成本或低价格低廉,且不带入杂质(其他合理答案均可) 4Fe2++O2+4H+===4Fe3++2H2O Fe3++3NH3·H2O===Fe(OH)3↓+3NH![]() MgSO4、CaSO4
MgSO4、CaSO4
【解析】废渣(含Fe2+、Fe3+的硫酸盐及少量CaO和MgO),将废渣溶解,溶解时加入的物质能溶解废渣但不能引进杂质;然后向溶液中加入A,A具有氧化性,能氧化亚铁离子但不能引进新的杂质且原料易得、成本低,应为空气中的氧气,然后向溶液中加入氨水,溶液中硫酸铁和氨水反应生成铵黄铁矾,同时溶液中镁离子、钙离子形成氢氧化钙、氢氧化镁、硫酸钙等会结晶析出,过滤分离得到铵黄铁矾和滤液;将滤液蒸发浓缩回收硫酸铵;将铵黄铁矾溶于水得到溶液,然后向溶液中加入氨水,得到氢氧化铁沉淀,然后过滤得到滤渣,将滤渣加热得到铁红。
(1)加速废渣溶解,可采用的措施有:将废渣粉碎、加热、搅拌等,故答案为:将废渣粉碎、加热、搅拌等;
(2)①物质A是氧化剂,具有氧化性,能氧化亚铁离子,但不能引进新的杂质且原料易得、成本低,氯气和二氧化锰都具有氧化性,但引进新的杂质且成本高,所以选取空气,故答案为:A;
②空气作为原料,成本低,不产生污染,不引入杂质,故答案为:原料易得,成本低,不产生污染,不引入杂质;
③氧化过程中发生反应的离子方程式为:4Fe2++O2+4H+═4Fe3++2H2O,故答案为:4Fe2++O2+4H+═4Fe3++2H2O;
(3)往铵黄铁矾溶液(含Fe3+)中加入氨水至pH为5时,铁离子与氨水反应生成氢氧化铁沉淀,反应的离子方程式为Fe3++3NH3·H2O===Fe(OH)3↓+3NH![]() ,故答案为:Fe3++3NH3·H2O===Fe(OH)3↓+3NH
,故答案为:Fe3++3NH3·H2O===Fe(OH)3↓+3NH![]() ;
;
(4)根据分析,回收所得的(NH4)2SO4晶体中可能含有的杂质有MgSO4、CaSO4,故答案为:MgSO4、CaSO4。


 字词句篇与同步作文达标系列答案
字词句篇与同步作文达标系列答案科目:高中化学 来源: 题型:
【题目】下列有关图示多肽的叙述,正确的是( )

A. 由5个氨基酸缩合而成 B. 形成过程中失去了3分子水
C. 有4种不同的侧链基团 D. 游离的氨基和羧基各1个
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】完成下面有关组成细胞主要化合物的概念图:

(1)写出图1中化合物的名称:①________②________③________④_______
(2)图1的②中被称为生命的燃料的是__________,脂质中构成细胞膜重要成分的是________,举一例说明③在生命活动所承担的功能:__________。
(3)图2为图1中④的一条长链,1、2、4的名称分别是________、_________、__________。该结构中特有的碱基名称是_________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】向猪膀胱内注入一半质量分数为30%的蔗糖溶液,扎紧入口,然后将其浸入质量分数为5%的蔗糖溶液中,每隔10 min称一次猪膀胱的重量,能正确表示测定结果的是下图中的
A.  B.
B. 
C.  D.
D. 
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某废催化剂含58.2%的SiO2、21.0%的ZnO、4.5%的ZnS和12.8%的CuS,某同学以该废催化剂为原料,回收其中的锌和铜。采用的实验方案如下:

已知:1.步骤①中发生的化学反应为非氧化还原反应 2.滤渣2的主要成分是SiO2和S,下列说法不正确的是
A. 步骤①,最好在通风橱中进行
B. 步骤①和③,说明CuS不溶于稀硫酸而ZnS溶于稀硫酸
C. 步骤③,涉及的离子反应为CuS+H2O2+2H+![]() Cu2++S+2H2O
Cu2++S+2H2O
D. 步骤②和④,均采用蒸发结晶的方式获取溶质
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】原子电子层数相同的X、Y、Z三种元素,若最高价氧化物的水化物酸性强弱为H3XO4<H2YO4<HZO4,则下列判断正确的是
A.非金属性强弱为X>Y>Z
B.原子半径为X<Y<Z
C.阴离子的还原性为X3->Y2->Z-
D.气态氢化物的稳定性为H3X>H2Y>HZ
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】A、B、C、D、E、F六种短周期元素,其原子序数依次增大,其中:C元素的原子最外层电子数是次外层电子数的三倍;A与D、C与F同主族;D是所在周期原子半径最大的主族元素,又知六种元素所形成的常见单质在常温常压下有三种是气体,三种是固体。请回答下列问题:
(1)元素D在周期表中的位置________________。
(2)写出B单质的电子式________________。
(3)C、D、F三种元素形成的简单离子的半径由大到小的顺序是________(用离子符号表示)。
(4)由A、B、C三种元素以原子个数比4∶2∶3形成化合物X,X中所含化学键类型有_________________________。
(5)若E是金属元素,其单质与氧化铁反应常用于焊接钢轨,请写出反应的化学方程式:__________________________________________________________。
若E是非金属元素,其单质在电子工业中有重要应用,请写出其氧化物溶于强碱溶液的离子方程式:_______________________________________________。
(6)FC2气体有毒,排放到大气中易形成酸雨,写出FC2与氧气和水蒸气反应的化学方程式_________________________________________________________。
(7)写出由A和D形成的化合物与水反应的化学方程式_____________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列试剂中无法鉴别对应物质的是
选项 | 物质 | 试剂 |
A | 乙醛 甲苯和CCl4 | 水 |
B | 甲烷 乙炔和四氯化碳 | 溴水 |
C | 乙醇 乙酸和乙酸乙酯 | 饱和碳酸钠溶液 |
D | 苯甲醇 苯甲醛和苯甲酸 | 酸性高锰酸钾溶液 |
A. A B. B C. C D. D
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com