

 .
.分析 元素在周期表中的位置,可知①是H,②是C,③是N,④是O,⑤是Na,⑥是Mg,⑦是Si,⑧是P,⑨是Cl,
(1)由①和②两种元素组成的相对分子质量为28的化合物为C2H4,元素⑧为P,原子序数为15;
(2)电子层越多,原子半径越大;同周期从左向右原子半径减小;
(3)非金属性越强,元素的最高价氧化物对应的水化物的酸性越强;
(4)非金属性越强,对应元素的气态氢化物越稳定.
解答 解:元素在周期表中的位置,可知①是H,②是C,③是N,④是O,⑤是Na,⑥是Mg,⑦是Si,⑧是P,⑨是Cl,
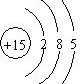
(1)由①和②两种元素组成的相对分子质量为28的化合物为C2H4,结构简式为CH2=CH2,元素⑧为P,原子序数为15,原子结构示意图为 ,
,
故答案为:CH2=CH2; ;
;
(2)电子层越多,原子半径越大;同周期从左向右原子半径减小,则③、④、⑤三种元素的原子半径由大到小的顺序是Na>N>O,
故答案为:Na>N>O;
(3)非金属性越强,元素的最高价氧化物对应的水化物的酸性越强,则③和⑧两种元素的最高价氧化物对应的水化物中酸性较强的是HNO3,
故答案为:HNO3;
(4)非金属性越强,对应元素的气态氢化物越稳定,非金属性Cl>P,元素⑧的气态氢化物比元素⑨的气态氢化物的稳定性较弱,
故答案为:弱.
点评 本题考查位置、结构与性质的关系,为高频考点,把握元素的位置、性质、元素化合物知识等为解答的关键,侧重分析与应用能力的考查,注意元素化合物知识及规律性知识的应用,题目难度不大.


科目:高中化学 来源: 题型:选择题

| A. | 铜电极上发生反应Cu-2e-=Cu2+ | |
| B. | 工作一段时间后,乙池的c(SO42-)减小 | |
| C. | 电流从铜极经过导线移向锌极 | |
| D. | 电池工作一段时间后,甲池的c(Zn2+)增加 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 向铝盐溶液中不断加入偏铝酸钠溶液 | |
| B. | 向盐酸中不断加入偏铝酸钠溶液 | |
| C. | 向氢氧化钠溶液中加铝盐溶液 | |
| D. | 向偏铝酸盐中下断加入盐酸 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| 实验操作 | 实验现象 | 实验结论 | |
| A | SO2通入Ba(NO3)2溶液中 | 不产生沉淀 | 亚硫酸的酸性比硝酸弱 |
| B | 气体X通入酸性KMnO4中 | 溶液褪色 | 气体X有漂白性 |
| C | 取少量某无色溶液,先滴加氯水,再加入少量苯,振荡、静置 | 溶液分层,下层呈紫红色 | 原无色溶液中一定有I- |
| D | 将铜片放入稀硝酸中,加热 | 产生大量气体溶液变为蓝色 | 稀硝酸具有强氧化性和酸性 |
| A. | A | B. | B | C. | C | D. | D |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | ①②④③ | B. | ①②④⑤ | C. | ②③④⑤ | D. | ①④③ |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 定容时观察液面仰视 | B. | 定容时观察液面俯视 | ||
| C. | 有少量NaOH溶液残留在烧杯中 | D. | 容量瓶中原来有少量蒸馏水 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 使石蕊变红的溶液中:Na+、K+、AlO2-、HCO3- | |
| B. | $\frac{c({H}^{+})}{c(O{H}^{-})}$=108的溶液中:Mg2+、Cu2+、SO42-、NO3- | |
| C. | 与Al反应能放出H2的溶液中:Fe2+、NH4+、NO3-、SO42- | |
| D. | 0.1 mol•L-1Fe2(SO4)3溶液中:Al3+、Ba2+、Cl-、OH- |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com