
1919年,Langmuir提出等电子原理:原子数相同、电子总数相同的微粒,互称为等电子体。等电子体的结构相似、物理性质相近。根据上述原理,下列微粒中,不互为等电子体的是
A.N2 和 CO B.CO2 和 N2O C.O3 和 CO2 D.CO32- 和 NO3-
 口算题卡加应用题集训系列答案
口算题卡加应用题集训系列答案 综合自测系列答案
综合自测系列答案科目:高中化学 来源:2015-2016学年安徽黄山屯溪一中高二下期中文科化学试卷(解析版) 题型:选择题
某工厂的废渣中混有少量的锌粉和氧化铜(其它成分不跟酸反应),跟废盐酸接触形成污水。若向该污水中撒入铁粉,反应后铁粉有剩余,所得溶液中一定含有的金属离子是
A.Fe2+、Cu2+ B.Cu2+、Zn2+ C.Zn2+、Fe2+ D.Zn2+、Fe3+
查看答案和解析>>
科目:高中化学 来源:2015-2016学年山东省高二下期中化学试卷(解析版) 题型:选择题
某中性有机物C6H12O6在稀硫酸作用下加热得到A和B两种物质,A在CuO加热条件下可转化为C,B和C都能发生银镜反应,则该中性有机物的结构可能有
A.1种
B.2种
C.3种
D.4种
查看答案和解析>>
科目:高中化学 来源:2016届湖南省等四校高三联考化学试卷(解析版) 题型:填空题
I.为有效控制雾霾,各地积极采取措施改善大气质量。有效控制空气中氮氧化物、碳氧化物和硫氧化物显得尤为重要。在汽车排气管内安装催化转化器,可将汽车尾气中主要污染物转化为无毒的大气循环物质。热化学反应方程式为 2NO(g)+2CO(g) N2(g)+2CO2(g) △=-746.5kJ• mol-1,将1.0 mol NO和1.0 mol CO充入一个容积为10L的密闭容器中,反应过程中物质浓度变化如图所示。
N2(g)+2CO2(g) △=-746.5kJ• mol-1,将1.0 mol NO和1.0 mol CO充入一个容积为10L的密闭容器中,反应过程中物质浓度变化如图所示。
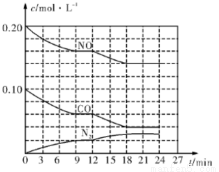
(1)CO在0〜9 min内的平均反应速率w(CO)= mol • L-1•min-1(保留两位有效数字);第12 min时改变的反应条件可能为 。
A.升高温度 B.减小压强 C.降低温度 D.加催化剂
(2)该反应在第24 min时已达到平衡状态,此时C02的体积分数为 (数值保留至小数点后一位),化学平衡常数K= (数值保留至小数点后一位)。
Ⅱ.能源的开发利用与人类社会的可持续发展息息相关。
(1)已知:Fe2O3(s)+3C(s) 2Fe(s)+3CO(g) △H1=a kJ • mol-1
2Fe(s)+3CO(g) △H1=a kJ • mol-1
CO(g) +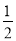 O2 (g)
O2 (g) CO2 (g) △H2=ckJ• mol-1
CO2 (g) △H2=ckJ• mol-1
4Fe(s)+3O2(g) 2Fe2O3 (s) △H3=c kJ • mol-1
2Fe2O3 (s) △H3=c kJ • mol-1
则C的燃烧热△H=________kJ•mol-1。
(2)依据原电池的构成原理,下列化学反应在理论上可以设计成原电池的是 (填序号)。
A.C(s )+CO2 (g)=2CO(g)
B.NaOH(aq) + HCl(aq)=NaCl(aq) +H2O(l)
C.2CO(g) +O2(g)=2CO2 (g )
D.2H2O(1 )=2H2(g)+O2(g )
(3 )若以熔融的K2CO3与CO2为反应的环境,依据所选反应设计成一个原电池, 请写出该原电池的负极反应: 。
查看答案和解析>>
科目:高中化学 来源:2016届湖南省等四校高三联考化学试卷(解析版) 题型:选择题
下表是25℃时某些盐的溶度积常数和弱酸的电离平衡常数,下列说法正确的是
化学式 | AgCl | Ag2CrO4 | CH3COOH | HC1O | H2CO3 |
KSp 或Ka | Ksp=1.8×10-10 | Ksp=2.0×10-12 | Ka=1.8×10 -5 | Ka=3.0×10-8 | Ka1=4.1×10一7 Ka =5.6×10-11 |
A.相同浓度CH3COONa和Na2CO3的混合液中,各离子浓度的关系有:
c(Na+ )>c(CO32- )>c(CH3COO一)>c(OH-)>c(H+)
B.向0.1 mol/LCH3COOH溶液中滴加NaOH溶液至溶液pH=5,此时 c(CH3COO) : c(CH3COO 一)=9 : 5
C.少量碳酸氢钠固体加入到新制的氯水中,c(HClO)增大
D.向浓度均为1×10-3mol/L的KC1和K2CrO4混合液中滴加1×10-3mol/L的AgNO3溶液,CrO42-先形成沉淀
查看答案和解析>>
科目:高中化学 来源:2016届湖南省等四校高三联考化学试卷(解析版) 题型:选择题
下列说法正确的是
A.可使用溴水鉴别植物油和汽油
B.利用二氧化碳制造全降解塑料,可以消除温室效应
C.“玉兔号”月球车上的太阳能电池的材料是硅
D.实验室金属钠失火时,可使用泡沫灭火器灭火
查看答案和解析>>
科目:高中化学 来源:2015-2016学年天津市高一下期中化学试卷(解析版) 题型:选择题
A、B、C、D、E均为短周期元素。A、B、C位于同一周期相邻位置,他们分别与D形成的分子中都有10个电子,且A和C的原子序数之比为3:4。E原子半径是短周期元素原子半径最大的。则下列叙述正确的是
A.C和D能形成D2C2的离子化合物
B.由A、D原子构成的分子的结构是正四面体
C.E和C只能形成E2C一种化合物
D.由A、B、C、D四种元素形成的化合物可以是离子化合物
查看答案和解析>>
科目:高中化学 来源:2015-2016学年天津市高一下期中化学试卷(解析版) 题型:选择题
已知X、Y、Z为三种原子序数相连的元素,最高价氧化物对应水化物的酸性相对强弱是:HXO4>H2YO4>H3ZO4。则下列说法正确的是
A.气态氢化物的稳定性:HX<H2Y<ZH3
B.非金属活泼性:Y<X<Z
C.离子半径:X-<Y2-<Z3-
D.原子序数:Z>Y>X
查看答案和解析>>
科目:高中化学 来源:2015-2016学年宁夏育才中学高一下期中化学试卷(解析版) 题型:选择题
如下图所示的装置的中,观察到电流计指正偏转,M棒变粗,N棒变细,并测得电解质溶液的质量减小,由此判断下表中所列M、N、P物质,其中可以成立的是( )
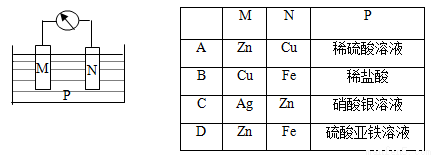
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com