
【题目】实验室有三瓶失去标签的试剂,分别是Na2CO3、NaCl、AgNO3。实验员选择了一种试剂用化学方法一次性就把它们区别开来了,这种试剂是:( )
A. 盐酸 B. 氢氧化钠溶液 C. 氯化钡溶液 D. 硝酸
科目:高中化学 来源: 题型:
【题目】氢气是未来最理想的能源,科学家最近研制出利用太阳能产生激光,并在二氧化钛(TiO2)表面作用使海水分解得到氢气的新技术2H2O![]() 2H2↑+O2↑.制得的氢气可用于燃料电池.试完成下列问题:太阳光分解海水时,实现了从________能转化为________能,二氧化钛作________生成的氢气,用于燃料电池时,实现________能转化为________能.分解海水的反应属于________反应(填“放热”或“吸热”).
2H2↑+O2↑.制得的氢气可用于燃料电池.试完成下列问题:太阳光分解海水时,实现了从________能转化为________能,二氧化钛作________生成的氢气,用于燃料电池时,实现________能转化为________能.分解海水的反应属于________反应(填“放热”或“吸热”).
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】常温下,用 0.1000molL﹣1NaOH溶液滴定 20.00mL0.1000molL﹣1CH3COOH溶液所得滴定曲线如图.下列说法正确的是( ) 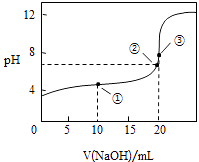
A.点①所示溶液中:c(CH3COO﹣)+c(OH﹣)=c(CH3COOH)+c(H+)
B.点②所示溶液中:c(Na+)=c(CH3COOH)+c(CH3COO﹣)
C.点③所示溶液中:c(Na+)>c(OH﹣)>c(CH3COO﹣)>c(H+)
D.滴定过程中可能出现:c(CH3COOH)>c(CH3COO﹣)>c(H+)>c(Na+)>c(OH﹣)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】为了除去氯化铝酸性溶液中的Fe3+ , 可在加热搅拌的条件下加入一种过量的试剂,过滤后再加入适量盐酸.这种试剂是( )
A.氨水
B.氧化铝
C.氢氧化钠
D.氢氧化铁
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列关于磷酸(H3PO4)的叙述错误的是( )
A. 磷酸的相对分子质量是98B. 磷酸的摩尔质量是98g
C. 1molH3PO4的质量是98gD. 1molH3PO4中含有4molO
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】镍镉(Ni﹣Cd)可充电电池在现代生活中有广泛应用.已知某镍镉电池的电解质溶液为KOH溶液,其充、放电按下式进行:Cd+2NiOOH+2H2O ![]() Cd(OH)2+2Ni(OH)2 . 有关该电池的说法正确的是( )
Cd(OH)2+2Ni(OH)2 . 有关该电池的说法正确的是( )
A.充电时阳极反应:Ni(OH)2﹣e﹣+OH﹣═NiOOH+H2O
B.充电过程是化学能转化为电能的过程
C.放电时负极附近溶液的碱性不变
D.放电时电解质溶液中的OH﹣向正极移动
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列反应既属于化合反应,又属于氧化还原反应的是( )
A. Fe +2 HCl = H2 ↑+ FeCl2 B. 2FeCl2 + Cl2 = 2FeCl3
C. CaO + H2O = Ca(OH)2 D. 2Fe(OH)3 = Fe2O3 + 3H2O
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】根据电化学知识回答下列问题:
(1)如图所示,在不同的电解质溶液中可以组成不同的电池。

①当电解质溶液为稀硫酸时,Fe电极是________(填“正”或“负”)极,其电极反应式为__________。
②当电解质溶液为NaOH溶液时,Al电极是________(填“正”或“负”) 极,其电极反应式为_________。
③若把铝改为锌,电解质溶液为浓硝酸,则Fe电极是______(填“正”或“负”)极,其电极反应式为_______________________________。
(2)请你利用原电池原理,设计实验,比较铜和银的金属活动性。画出实验装置图,标出正负极、电子流动方向。________

查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】自来水一般是用少量的氯气消毒。如果实验室中临时没有蒸馏水,可以用自来水配制某些急需的药品,但有些药品若用自来水配制,则明显会导致药品变质。下列哪些药品不能用自来水配制
A. Na2SO4 B. NaCl C. AgNO3 D. KNO3
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com