
| A. | 元素的非金属性:X<Y<Z | B. | X、Y、Z依次位于ⅤA族、ⅥA族、ⅦA族 | ||
| C. | 阴离子的还原性:X->Y2->Z3- | D. | 气态氢化物的稳定性:HX>H2Y>ZH3 |
分析 同周期元素从左到右,非金属性逐渐增强,则对应的最高价氧化物水化物的酸性逐渐增强,酸性由弱到强的顺序是:HXO4>H2YO4>H3ZO4,则非金属性:Z<Y<X,原子序数Z<Y<X,以此解答该题.
解答 解:同周期元素从左到右,非金属性逐渐增强,则对应的最高价氧化物水化物的酸性逐渐增强,酸性由弱到强的顺序是:HXO4>H2YO4>H3ZO4,则非金属性:Z<Y<X,原子序数Z<Y<X.
A.同周期元素原子序数Z<Y<X,同周期元素从左到右,非金属性逐渐增强,则非金属性Z<Y<X,故A错误;
B.由化学式可知X、Y、Z的最高价分别为+7价、+6价、+5价,则依次位于ⅦA族、ⅥA族、ⅤA族,故B错误;
C.非金属性Z<Y<X,元素的非金属性越强,对应单质的氧化性越强,则阴离子的还原性越弱,故C错误;
D.同周期元素原子序数Z<Y<X,同周期元素从左到右,非金属性逐渐增强,对应氢化物的稳定性逐渐增强,故D正确,
故选D.
点评 本题考查位置结构性质关系应用,明确最高价氧化物的酸性推出非金属性的强弱是解答本题的关键,难度不大.


科目:高中化学 来源: 题型:选择题
| A. | 只有②③④⑤ | B. | 只有①③④⑤ | C. | ①②③④⑤ | D. | 只有①②③⑤ |
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
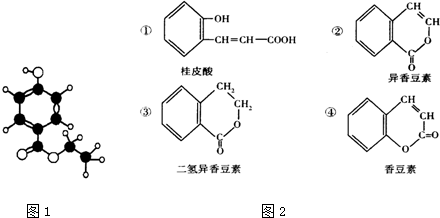
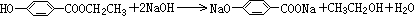 ;
; ;
;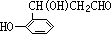 .
.查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 3mol•L-1 | B. | 0.2mol•L-1 | C. | 0.3mol•L-1 | D. | 0.1mol•L-1 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 6.02×1022个H2SO4分子在水中可电离生成2NA个H+ | |
| B. | 在0℃、101 kPa时,22.4 L氢气中含有NA个氢原子 | |
| C. | 14 g氮气中含有7NA个电子 | |
| D. | NA个一氧化碳分子和0.5 mol甲烷的质量比为7:4 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题

查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | NaCl | B. | NaBr、NaI、NaCl | C. | NaBr、NaI | D. | NaCl、I2 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
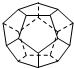 德国和美国科学家首先制出由20个碳原子组成的空心笼状分子C20,该笼状结构是由许多正五边形构成(如图).请回答:C20分子共有12个正五边形,共有30条棱边,C20晶体属于分子晶体 (填晶体类型).
德国和美国科学家首先制出由20个碳原子组成的空心笼状分子C20,该笼状结构是由许多正五边形构成(如图).请回答:C20分子共有12个正五边形,共有30条棱边,C20晶体属于分子晶体 (填晶体类型).查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com