
��������E�������ڻ�ױƷ���������գ��ֲ�����ҩ�ȡ���������ķ�Ӧ·�߿���ʵ�ֱ���������Ʊ������dz������������ۺ����á�
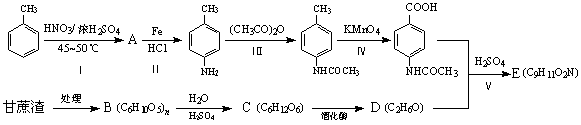
��ش��������⣺
��1����Ӧ��Ļ�ѧ����ʽ�� ��
��2��B��������_____________��C�к��еĹ����������� ��
��3���ڷ�Ӧ���У�����ȡ����Ӧ���ǣ�����ţ�________��
��4��д����Ӧ���Ļ�ѧ����ʽ�� ��
��5�����������ж���ͬ���칹�壬���У�����ֱ�����ڱ����ϣ������ϵ�һ��ȡ����ֻ��һ�ֵ�������ͬ���칹��Ľṹ��ʽΪ�� ��
 �ǻ�С��ϰϵ�д�
�ǻ�С��ϰϵ�д�
| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
���ڽ������Һ������������������ȷ����
A����Һ�ʵ����ԣ�������е��
B����Һ��������һ�������磬�����з�ɢ�������е��
C����Һ�з�ɢ����������ֽ�������з�ɢ������������ֽ
D����Һ��ͨ��һ������û��������������ͨ��һ�����߳��������Ĺ��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
1���ij��̬����2����Ȼ��ⷢ���ӳɷ�Ӧ�����ܺ�6�����������ȡ����Ӧ���ɴ˿��Զ϶�ԭ��̬���ǣ��������������ͬ�����²ⶨ��
A����Ȳ B����Ȳ C����Ȳ D������ϩ
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�

(3)����������NaOHŨ��Һ�ڼ��������·�Ӧ�����ӷ���ʽΪ_______________________��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
��NAΪ����٤��������ֵ������˵���������
A��1 mol 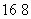 OD�� ���Ӻ��е����ӡ���������Ϊ9NA
OD�� ���Ӻ��е����ӡ���������Ϊ9NA
B��3.6 gʯī��C60�Ļ�����У����е�̼ԭ����Ϊ0.3NA
C������4.6 g��Ԫ�صĹ������ƺ������ƵĻ�����У�������������Ϊ0.3NA
D����״���£�4.48 L���麬�еķ�����Ϊ0.2NA
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
�����£����и���������ָ����Һ��һ���ܴ����������
A.���ȳʺ�ɫ����Һ�У�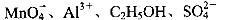
B.�����µ���Һ��
C. O.1 mol/L AgNO3��Һ��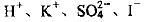
D.���뱽������ɫ����Һ��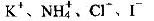
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
��һ�������£��������ӵĻ�ԭ��˳��Cl��<Br��<Fe2+<I��<SO2���ɴ��ж����¸���Ӧ����Һ�������������� �� ��
A��2Fe3++SO2+2H2O===2Fe2++SO42��+4H+
B��2Br��+4H++SO42��===SO2+Br2+2H2O
C��2Fe2++Cl2===2Fe3+2Cl��
D��I2+SO2+2H2O===4H++SO42��+2I��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
���ȸʯ��һ�ֺ�ͭ��ʯ����ͭ��̬ΪCuCO3��Cu(OH)2��CuSiO3��2H2O��ͬʱ����SiO2��FeCO3��Fe2O3��Al2O3�����ʡ�����Ϊԭ����ȡ����ͭ�Ĺ���������ͼ��

�� ��ɲ������ϡ������CuSiO3��2H2O��Ӧ�Ļ�ѧ����ʽ:
CuSiO3��2H2O+H2SO4=CuSO4 +_______+H2O��˫��ˮ��������____ ��
�� ����ڵ�����ҺpH,����ѡ�õ��Լ���______
A. CuO B. Fe2O3 C.Al2O3 D Cu(OH)2
�� �й��������↑ʼ��������ȫ������pH���±���
| �������� | Al(OH)3 | Fe(OH)3 | Fe(OH)2 | Cu(OH)2 |
| ��ʼ������pH | 3.3 | 1.5 | 6.5 | 4.2 |
| ������ȫ��pH | 5.2 | 3.7 | 9.7 | 6.7 |
������У�����pH=4ʱ����������B�ijɷֵĻ�ѧʽΪ ����ҺB�г�Cu2+��, �����еĽ����������� ��
�� ����ҺBͨ�� �� �����˵Ȳ����ɵõ�����ͭ���塣
�� �ⶨ����ͭ����ᾧˮ�ĺ���ʱ��Ӧ�������______�����ա�����ʧˮ��,���ڿ�������ȴ�������ⶨ���__ ___(�ƫ�ߡ�����ƫ�͡����䡱)��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
���л�ѧʵ�����ע�ⰲȫ������˵������ȷ���ǣ� ��
A.�������ὦ�����У�Ӧ�����ô���ˮ��ϴ����ϴ��գ�۾�
B.������Ũ����Һմ��Ƥ���ϣ�Ӧ�����ô�����ˮ��ϴ
C.�����Թܻ��ձ�ʱ��Ӧ���Ȳ�������ϵ�ˮ
D.����������Һʱ����������Ͳ�м���һ�������ˮ�����ڽ�����������������Ũ����
�鿴�𰸺ͽ���>>
����ѧУ��ѡ - ��ϰ���б� - �����б�
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com