
| A. | 制造普通水泥和玻璃的主要原料都用到石灰石 | |
| B. | 工业上制玻璃不会有温室气体的排放 | |
| C. | 玻璃钢是将玻璃纤维和高分子材料复合而成的复合材料 | |
| D. | “中国”的英文单词叫China,这是由于中国制造的某种物质驰名世界,这种物质是陶瓷 |
分析 A、制造水泥用黏土和石灰石,制造玻璃用碳酸钠和石灰石和石英;
B、取玻璃时碳酸钠和二氧化硅反应生成硅酸钠和二氧化碳;
C、玻璃钢是复合材料;
D、在英文中“瓷器(china)”与中国(China)同为一词.
解答 解:A、制造水泥用黏土和石灰石,制造玻璃用碳酸钠和石灰石和石英,都用石灰石,故A正确;
B、制取玻璃时碳酸钠和二氧化硅反应生成硅酸钠和二氧化碳,产生二氧化碳,二氧化碳是温室气体,故B错误;
C、玻璃钢是复合材料,是将玻璃纤维和高分子材料复合而成的,故C正确;
D、中国是瓷器的故乡,瓷器是汉族劳动人民的一个重要的创造.瓷器的发明是汉民族对世界文明的伟大贡献,在英文中“瓷器(china)”与中国(China)同为一词,故D正确;
故选B.
点评 本题考查了无机非金属材料中的硅酸盐材料,难度不大,有助于提高学习的积极性,提升民族自豪感.


科目:高中化学 来源: 题型:选择题
| A. | 同质量不同密度的C2H4和CO | B. | 同温度同体积的C2H6和NO2 | ||
| C. | 同温度同密度的CO2和N2 | D. | 同体积同压强的N2和C2H2 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | KH的水溶液呈碱性 | B. | KH中氢离子可以被还原为氢气 | ||
| C. | KH是一种强氧化剂 | D. | KH中的氢离子是裸露的质子 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| 选项 | 陈述Ⅰ | 陈述Ⅱ |
| A | Fe2O3是红棕色粉末 | Fe2O3常用作红色涂料 |
| B | SiO2是两性氧化物 | SiO2可和HF反应 |
| C | Al2O3难溶于水 | Al2O3可用作耐火材料 |
| D | SO2有氧化性 | SO2可使溴水褪色 |
| A. | A | B. | B | C. | C | D. | D |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
| 实验序号 | 甲 | 乙 | 丙 |
| 合金质量/g | 8.8 | 17.6 | 22.0 |
| 气体体积/L | 2.24 | 4.48 | 4.48 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
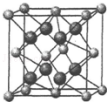 氟在自然界中常以CaF2的形式存在.
氟在自然界中常以CaF2的形式存在.查看答案和解析>>
科目:高中化学 来源: 题型:填空题
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com