
| A、a=b-15 |
| B、a=b-29 |
| C、a=b-9 |
| D、a=b-5 |


科目:高中化学 来源: 题型:
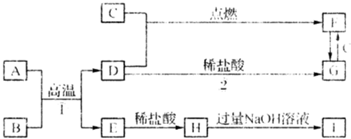
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、是离子化合物,含有离子键和共价键 |
B、电子式是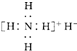 |
| C、与水反应时,是还原反应 |
| D、固体投入少量的水中,有两种气体产生 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、由于金属键具有方向性与饱和性,所以金属在外加电场作用下导电 |
| B、金属键是金属阳离子与自由电子间的相互作用 |
| C、氢键、配位键都是特殊的共价键 |
| D、离子晶体中只存在离子键 |
查看答案和解析>>
科目:高中化学 来源: 题型:
A Z |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、航天飞机上使用的隔热陶瓷瓦,大多是以碳纤维做基体的新型复合材料 |
| B、盐卤点豆腐、血液透析均与胶体的性质有关 |
| C、绿色化学的核心是应用化学原理对环境污染进行治理 |
| D、工业制备玻璃、水泥、陶瓷用到的共同原料是石灰石 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、35Cl原子所含质子数为18 | ||
B、
| ||
| C、3.5g35Cl2气体的体积为1.12L | ||
| D、已知自然界中氯元素的平均相对原子质量为35.5,则37Cl的质量分数为25% |
查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
| 除去悬浮 |
| 杂质 |
| 浓缩 |
| 氧化剂 |
| 氧化 |
| 热空气 |
| Na2CO3溶液 |
| 吸收 |
| H2SO4 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com