
【题目】常温下,0.2mol/L的一元碱BOH与等浓度的HCl溶液等体积混合后,所得溶液中部分微粒组分及浓度如图所示,下列说法正确的是( )
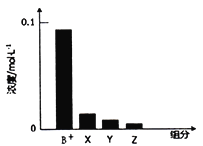
A. BOH为强碱 B. 该混合液pH=7
C. 图中X表示BOH,Y表示H+,Z表示OH- D. 该混合溶液中:c(Cl-)=c(Y)+c(B+)
【答案】D
【解析】0.2mol/L的一元碱BOH与等浓度的盐酸等体积混合后,HCl+BOH=BCl+H2O,所得溶液中B+浓度小于0.1mol/L,说明在溶液中存在B++H2O![]() H++BOH,BOH为弱碱,BCl溶液呈酸性,则c(OH-)<c(H+),一般来说,盐类的水解程度较低,则有c(B+)>c(H+),所以有:c(Cl-)=0.1mol/L>c(B+)>c(H+)>c(BOH)>c(OH-)即X表示H+,Y表示BOH,Z表示OH-,溶液中存在物料守恒为:c(Cl-)=c(B+)+c(BOH)。
H++BOH,BOH为弱碱,BCl溶液呈酸性,则c(OH-)<c(H+),一般来说,盐类的水解程度较低,则有c(B+)>c(H+),所以有:c(Cl-)=0.1mol/L>c(B+)>c(H+)>c(BOH)>c(OH-)即X表示H+,Y表示BOH,Z表示OH-,溶液中存在物料守恒为:c(Cl-)=c(B+)+c(BOH)。
A.BOH为弱碱,选项A错误;B、所得溶液为BCl溶液,为强酸弱碱盐溶液,溶液呈酸性,pH<7,选项B错误;C、图中X表示H+,Y表示BOH,Z表示OH-,选项C错误;D、溶液中存在物料守恒为:c(Cl-)=c(B+)+c(BOH),选项D正确。答案选D。


 名校课堂系列答案
名校课堂系列答案科目:高中化学 来源: 题型:
【题目】下列说法中不正确的是( )
A.硫单质与金属铁反应生成FeS,体现了硫单质的氧化性
B.SO2能使酸性KMnO4、氯水褪色,说明SO2具有漂白作用
C.SO2既有还原性,又有氧化性
D.医疗上常用BaSO4作X射线透视的“钡餐”
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】SCR技术可有效降低柴油发动机尾气中NOx的排放。SCR(选择性催化还原)工作原理如图所示。
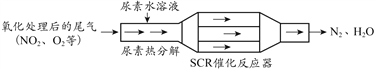
(1)汽车尾气直接排放会造成_______
a. 硝酸型酸雨 b. 硫酸型酸雨 c. 臭氧层空洞
(2)尿素[CO(NH2)2]水溶液热分解为NH3和CO2,反应器中NH3可以还原NO2,起到转化有害物质为无害物质的作用,已知参加反应的氨气与NO2的体积比为4:3,其反应方程式为_________。
(3)根据元素守恒,最终处理产物除了N2和H2O,还有_______。
(4)若通入尾气中含67.2L NO2(标准状况),则与氨气完全反应转移电子数为_____mol。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】石油产品中除含有H2S外,还含有各种形态的有机硫,如COS、CH3SH。回答下列问题:
(1)CH3SH(甲硫醇)的电子式为________。
(2)一种脱硫工艺为:真空K2CO3—克劳斯法。
①K2CO3溶液吸收H2S的反应为K2CO3+H2S=KHS+KHCO3,该反应的平衡常数的对数值为lgK=_____(已知:H2CO3 lgK1=-6.4,lgK2=-10.3;H2SlgK1=-7,lgK2=-19)。
②已知下列热化学方程式:
a.2H2S(g)+3O2(g)=2SO2(g)+ 2H2O(l) △H1=-1172kJ/mol
b.2H2S(g)+O2(g)=2S(s)+2H2O(l) △H2=-632kJ/mol
克劳斯法回收硫的反应为SO2和H2S气体反应生成S(s),则该反应的热化学方程式为__________。
(3)Dalleska等人研究发现在强酸溶液中可用H2O2氧化COS。该脱除反应的化学方程式为______________。
(4)COS水解反应为COS(g)+H2O(g)![]() CO2(g)+H2S(g) △H=-35.5kJ/mol。
CO2(g)+H2S(g) △H=-35.5kJ/mol。
用活性α-Al2O3催化,在其它条件相同时,改变反应温度,测得COS水解转化率如图1所示;某温度时,在恒容密闭容器中投入0.3molH2O(g)和0.1molCOS,COS的平衡转化率如图2所示。
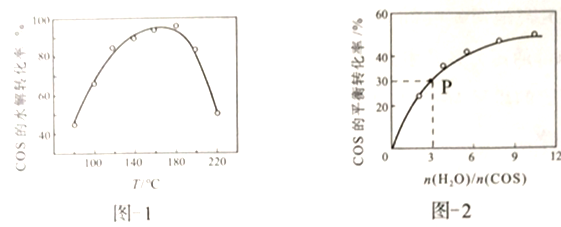
①图1活性α-Al2O3催化水解,随温度升高转化率先增大后又减小的可能原因是________。
②由图2可知,P点时平衡常数为K=______(填数字)。
③活性α-Al2O3催化水解,为提高COS的转化率可采取的措施是____________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列有关生活生产中的叙述合理的是
A. 打开啤酒瓶的瓶盖,大量的气泡冒出来,该现象不能用勒夏特列原理解释
B. 硫酸工业中SO2转化为SO3时采用常压,是因为增大压强不会提高SO2的转化率
C. 工业上合成氨采用500℃左右的温度,其原因是适当加快NH3的合成速率,催化剂在500℃左右时其活性最好
D. 氯碱工业:用离子交换膜电解槽电解时,往阳极室注入经过精制的NaCl溶液,往阴极室注入稀氢氧化钠溶液(或去离子水)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】如图是某学校实验室从化学试剂商店买回的硫酸试剂标签上的部分内容。 据此下列说法错误的是
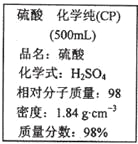
A. 该硫酸具有强烈的腐蚀性,应放于危险化学用品柜中妥善保管
B. 取10 mL该硫酸于烧杯中,再加等体积的水,可配得49%的硫酸
C. 配制200mL4.6 mol·L-1的稀硫酸需取该硫酸50 mL
D. 该硫酸与等质量的水混合所得溶液的物质的量浓度小于9.2 mol·L-1
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】我国某些地区曾发生用石蜡油等工业用油加工大米的“毒米事件”,威胁人民健康。食用油和石蜡油虽然都称作“油”,但从化学组成和分子结构看,它们是完全不同的。下列说法正确的是( )
A.食用油属于纯净物,石蜡油属于混合物
B.食用油属于酯类,石蜡油属于烃类
C.食用油属于有机物,石蜡油属于无机物
D.食用油属于高分子化合物,石蜡油属于小分子化合物
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】我国古代在西汉《淮南子·万毕术》一书中有湿法炼铜的文字记载:“曾青得铁则化铜”铜金属被广泛地应用于电力、电子、交通、轻工、新兴产业等领域。
回答下列问题:
(1)铁原子的外围电子排布图为___________。
(2)向FeCl3溶液加入KSCN溶液形成K3[Fe(SCN)6]血红色溶液。
①写出与SCN-离子互为等电子体的合理分子或离子:_____________。(两个)
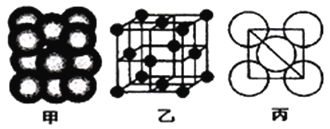
②铁原子的堆积方式如右图(甲)所示,其晶胞特征如右图(乙)所示,原子之间相互位置关系的平面图如右图(丙)所示;已知铁原子半径rpm,铁晶胞空间利用率为:____________。(用字母π表示)
(3)含有Fe2+的水溶液可以用K3[Fe(CN)6]于实验室的定性检验,检验Fe2+离子的离子方程式为:___________。
(4)一水合硫酸四氨合铜[Cu(NH3)4]SO4·H2O为蓝色正交晶体,常用作杀虫剂、媒染剂,在碱性镀铜中也常用作电镀液的主要成分,在工业上用途广泛。
①[Cu(NH3)4]SO4·H2O中非金属元素H、N、O的电负性由大到小的顺序为:___________。(用元素符号作答)
②[Cu(NH3)4]SO4·H2O晶体中存在的化学键有___________ (填编号)
a金属键 b离子键 c氢键 d配位键 e极性键 f非极性键
③NH3分子的VSEPR模型为:___________;SO42-中S为___________杂化。
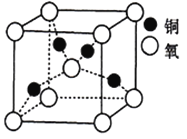
(5)铜的某种氧化物晶胞结构如图所示,若该晶胞的边长为acm,则该氧化物的密度为______g/cm3(设阿伏加德罗常数的值为NA)。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】有下列三个反应:
①Cl2+FeI2=FeCl2+I2
②2Fe2++Br2=2Fe3++2Br-
③Co2O3+6HCl=2CoCl2+Cl2↑+3H2O
下列说法正确的是( )
A. 反应①②③中的氧化产物分别是I2、Fe3+、CoCl2
B. 根据以上方程式可以得到氧化性:Cl2>Fe3+>Co2O3
C. 在反应③中当1 mol Co2O3参加反应时,2 mol HCl被氧化
D. 可以推理得到Cl2+FeBr2 =FeCl2+Br2
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com